Osmolariteetin kaava, miten se lasketaan ja ero Osmolaliteettiin
osmolaarisuus on parametri, joka mittaa kemiallisen yhdisteen konsentraatiota litraan liuosta, kunhan se vaikuttaa mainitun liuoksen osmoottiseen paineeseen tunnettuun kolligatiiviseen ominaisuuteen.
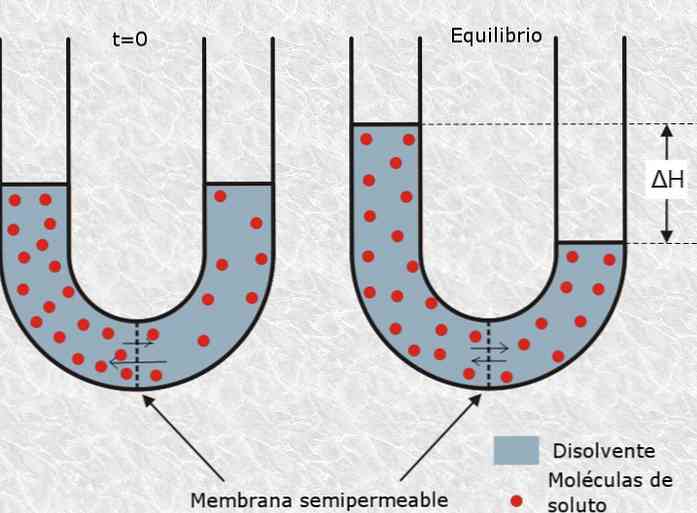
Tässä mielessä liuoksen osmoottinen paine viittaa paineen määrään, jota tarvitaan osmoosiprosessin hidastamiseksi, joka määritellään liuotinhiukkasten selektiiviseksi siirtymiseksi puoliläpäisevän tai huokoisen kalvon avulla liuoksesta. pienempi konsentraatio konsentraatioon.
Myös yksikkö, jota käytetään liukenevien hiukkasten määrän ilmaisemiseen, on osmoli (jonka symboli on Osm), joka ei kuulu kansainväliseen yksikköjen järjestelmään (SI), jota käytetään lähes koko maailmassa. Niinpä liuoksessa olevan liuoksen konsentraatio määritetään osmolien yksikköinä litraa kohti (Osm / l).
indeksi
- 1 Kaava
- 1.1 Osmolaarisuuskaavan muuttujien määrittely
- 2 Miten se lasketaan?
- 3 Osmolaarisuuden ja osmolaliteetin erot
- 4 Viitteet
kaava
Kuten aiemmin mainittiin, osmolaarisuus (tunnetaan myös nimellä osmoottinen konsentraatio) ilmaistaan yksiköinä, jotka on määritelty Osm / l: ksi. Tämä johtuu sen suhteesta osmoottisen paineen määrittämiseen ja liuottimen diffuusion mittaamiseen osmoosilla.
Käytännössä osmoottinen pitoisuus voidaan määrittää fyysisenä määränä osmometrin avulla.
Osmometri on väline, jota käytetään liuoksen osmoottisen paineen mittaamiseen sekä muiden kolligatiivisten ominaisuuksien (kuten höyrynpaineen, kiehumispisteen nousun tai jäätymispisteen masennuksen) määrittämiseen. liuoksen osmolaarisuudesta.
Tällä tavalla tämän mittausparametrin laskemiseksi käytetään seuraavaa kaavaa, jossa otetaan huomioon kaikki tekijät, jotka voivat vaikuttaa tähän ominaisuuteen..
Osmolariteetti = ΣφminänminäCminä
Tässä yhtälössä osmolaarisuus muodostetaan summana, joka saadaan kertomalla kaikki arvot, jotka on saatu kolmesta eri parametrista, jotka määritellään alla.
Määritellään muuttujat osmolaarisuuskaavassa
Ensinnäkin on osmoottinen kerroin, jota edustaa kreikkalainen kirjain φ (phi), joka selittää, kuinka pitkälle ideaalisen käyttäytymisen ratkaisu siirtyy pois, tai toisin sanoen, ei-idealiteetin aste, jonka soluutti ilmenee liuoksessa.
Yksinkertaisimmalla tavalla φ viittaa liuenneen aineen dissosiaatioasteeseen, jonka arvo voi olla nollan ja yhden välillä, jolloin yksikön maksimiarvo edustaa 100%: n dissosiaatiota; eli absoluuttinen.
Joissakin tapauksissa - kuten sakkaroosina - tämä arvo ylittää yhtenäisyyden; kun muissa tapauksissa, kuten suoloissa, sähköstaattisten vuorovaikutusten tai voimien vaikutus aiheuttaa osmoottisen kertoimen, jonka arvo on pienempi kuin yhtenäisyys, vaikka absoluuttinen dissosiointi tapahtuu.
Toisaalta n: n arvo ilmaisee hiukkasten määrän, jossa molekyyli voidaan hajottaa. Ionisten lajien tapauksessa annetaan esimerkkinä natriumkloridi (NaCl), jonka arvo n on kaksi; kun taas ionisoimattomassa glukoosimolekyylissä n: n arvo on yhtä kuin yksi.
Lopuksi c: n arvo edustaa liuenneen aineen konsentraatiota, ilmaistuna molaarisina yksikköinä; ja alaindeksi i viittaa tietyn liuoksen identiteettiin, mutta sen on oltava sama, kun kerrotaan edellä mainitut kolme tekijää ja siten saadaan osmolaarisuus.
Miten se lasketaan?
Jos kyseessä on ioninen yhdiste KBr (tunnetaan kaliumbromidina), jos sinulla on liuos, jonka konsentraatio on 1 mol / l KBr: tä vedessä, päätellään, että sen osmolaarisuus on 2 osmol / l..
Tämä johtuu sen vahvasta elektrolyyttimerkistä, joka suosii sen täydellistä hajoamista vedessä ja mahdollistaa kahden itsenäisen ionin vapautumisen (K+ ja Br-) joilla on jonkin verran sähkövaraa, niin että kukin KBr-mooli vastaa kahta osmolia liuoksessa.
Analogisesti, liuokselle, jonka konsentraatio on 1 mol / l BaCl2 (tunnetaan bariumkloridina) vedessä, sen osmolaarisuus on 3 osmol / l.
Tämä johtuu siitä, että kolme itsenäistä ionia vapautuu: Ba-ioni2+ ja kaksi Cl-ionia-. Sitten jokainen mooli BaCl2 vastaa kolme osmolia liuoksessa.
Toisaalta ei-ioniset lajit eivät mene tällaiseen dissosioitumiseen ja ovat peräisin yhdestä osmolista jokaiselle liuenneelle moolille. Kun kyseessä on glukoosiliuos, jonka pitoisuus on 1 mol / l, tämä vastaa 1 osmol / l liuosta.
Osmolaarisuuden ja osmolaliteetin erot
Osmoli määritellään hiukkasten lukumääräksi, joka liuotetaan tilavuuteen, joka on 22,4 l liuotinta, ja jonka lämpötila on 0 ° C ja joka aiheuttaa osmoottisen paineen muodostumisen, joka on yhtä suuri kuin 1 atm. On huomattava, että näitä hiukkasia pidetään osmoottisesti aktiivisina.
Tässä mielessä osmolaarisuus ja osmolaalisuus tunnetaan samassa mittauksessa: liuoksessa olevan liuoksen konsentraatio tai toisin sanoen liuoksen kokonaishiukkasten pitoisuus liuoksessa.
Osmolariteetin ja osmolaliteetin välillä vallitseva perustavanlaatuinen ero on yksiköissä, joissa kukin on edustettuna:
Osmolaarisuus ilmaistaan aineen määränä liuoksen tilavuutta kohti (ts. Osmol / l), kun taas osmolaliteetti ilmaistaan aineen määränä liuottimen massaa kohti (ts. Osmol / kg liuosta).
Käytännössä molempia parametreja käytetään välinpitämättömästi, jopa ilmenemällä eri yksiköissä, koska eri mittausten kokonaiskokojen välillä on epäasianmukainen ero..
viittaukset
- Wikipedia. (N.D.). Osmoottipitoisuus. Haettu osoitteesta es.wikipedia.org
- Chang, R. (2007). Kemia, yhdeksäs painos. Meksiko: McGraw-Hill.
- Evans, D. H. (2008). Osmoottinen ja ioninen säätely: solut ja eläimet. Haettu osoitteesta books.google.co.ve
- Potts, W. T. ja Parry, W. (2016). Osmoottinen ja ioninen asetus eläimissä. Haettu osoitteesta books.google.co.ve
- Armitage, K. (2012). Tutkimukset yleisessä biologiassa. Haettu osoitteesta books.google.co.ve


