Kalsiumhydroksidikaava, ominaisuudet, reaktiivisuus ja käyttö
kalsiumhydroksidi, tunnetaan myös nimellä hydratoitu kalkki tai sammutettu kalkki, on epäorgaaninen yhdiste, jolla on kaava Ca (OH)2.
Kalsiumhydroksidi käyttää polymeerirakennetta, kuten kaikki metallihydroksidit, joka on identtinen magnesiumhydroksidin (Mg (OH)) kanssa.2) tunnetaan myös nimellä brucita.
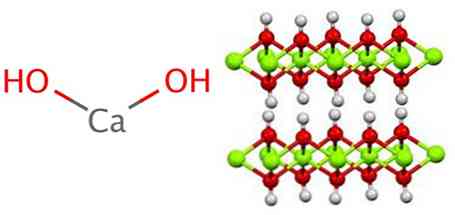
Voidaan nähdä, että tässä rakenteessa muodostuu vetysiltoja. Kalsiumhydroksidi syntetisoidaan teollisesti saattamalla kalsiumoksidi, joka tunnetaan myös nimellä kalkki tai kalkki, vedellä seuraavan reaktion mukaisesti:
CaOH + H2O → Ca (OH)2
Se valmistetaan myös laboratoriossa vesipitoisen kalsiumkloridin ja natriumhydroksidin välisellä reaktiolla.
Kalsiumhydroksidi esiintyy luonnollisesti, mutta harvoin sen mineraalimuodossa portlandiittina, jota esiintyy joissakin tulivuoren ja metamorfisissa kivissä. (Kalsiumhydroksidikaava - kalsiumhydroksidin käyttö, ominaisuudet, rakenne ja kaava, 2005-2017).
Tämä yhdiste on yleisesti saatavilla myös sementti-, liuotin- ja teollisuuspuhdistusaineissa (kuten rakennustuotteissa), lattianpoistimissa, tiilipuhdistimissa, sementin sakeuttamisaineissa ja monissa muissa..
Vesiliuosta kutsutaan tavallisesti limewateriksi. Kalkkivesi valmistetaan sekoittamalla kalsiumhydroksidia puhtaassa vedessä ja suodattamalla Ca (OH): n ylimäärä.2 ei ole liuennut.
Kun kalkkivesiin lisätään ylimääräistä kalsiumhydroksidia, saadaan kalsiumhydroksidihiukkasten suspensio, joka antaa sille maidon ulkonäön, jolloin siinä on tavallinen kalkkimaidon nimi. Kalkin tai kyllästetyn kalkkiliuoksen (kalkkivesi) pH on 12,3, joka on perusluonteinen.
Kalsiumhydroksidin fysikaaliset ja kemialliset ominaisuudet
Kalsiumhydroksidi on valkoinen tai väritön jauhe, josta puuttuu haju. Vesipitoisessa liuoksessa (tyydyttyneet liuokset) sillä on maitomainen ulkonäkö liukenemattoman kalsiumhydroksidin supernatantin vuoksi.
Tyydyttymättömät liuokset ovat tavallisesti kirkkaita ja värittömiä liuoksia, joilla on lievä maanläheinen haju ja katkera alkalinen maku kalsiumhydroksidista. Yhdisteen ulkonäkö on kuvattu kuviossa 3 (Royal Society of Chemistry, 2015).

Kalsiumhydroksidin molekyylipaino on 74,093 g / mol ja tiheys 2,211 g / cm3 kiinteässä tilassa. Sen sulamispiste on 580 astetta. Se liukenee huonosti veteen, sillä se pystyy liuottamaan 1,89 grammaa litraa kohti 0 ° C: ssa, 1,73 grammaa litrassa 20 ° C: ssa ja 0,66 grammaa litraa kohti 100 ° C: ssa..
Se liukenee glyseroliin ja happoliuoksiin. Se on liukenematon alkoholiin (National Biotechnology Information, S.F.).
Kalsiumhydroksidi liuotetaan osittain veteen, jolloin saadaan liuosta, jota kutsutaan limewateriksi, joka on kohtuullinen emäs. Kalkkivesi tai Ca (OH)2 (aq) Se reagoi happojen kanssa suolojen muodostamiseksi ja voi hyökätä joitakin metalleja, kuten alumiinia. Kalkkivesi reagoi helposti hiilidioksidin kanssa kalsiumkarbonaatin muodostamiseksi.
Ca (OH)2 + CO2 → CaCO3 + H2O
Nitroparafiinit, nitrometaani, nitropropaani jne. Muodostavat suoloja epäorgaanisten emästen, kuten kalsiumhydroksidin, kanssa. Nämä kuivat suolat ovat räjähtäviä. Yhdiste on kemiallisesti samanlainen kuin natriumhydroksidi (NaOH) tai natriumoksidi (Na2O). Nämä neutraloivat hapot eksotermisesti suolojen ja veden muodostamiseksi.
Näiden materiaalien sekoittaminen veteen voi aiheuttaa vaarallisia määriä lämpöä, kun pohja liukenee tai laimentuu. Alustat reagoivat tiettyjen metallien (kuten alumiinin ja sinkin) kanssa muodostaen metallioksideja tai -hydroksideja ja tuottavat vetykaasua.
Emäkset voivat käynnistää polymerointireaktioita polymeroituvissa orgaanisissa yhdisteissä, erityisesti epoksideissa. Syttyviä ja / tai myrkyllisiä kaasuja voidaan tuottaa ammoniumsuolojen, nitridien, halogenoitujen orgaanisten aineiden, erilaisten metallien, peroksidien ja hydroperoksidien kanssa. Tämän tyyppinen yhdiste toimii usein katalysaattorina (Chemical Datasheet CALCIUM HYDROXIDE, S.F.).
Reaktiivisuus ja vaarat

Kalsiumhydroksidi on stabiili yhdiste, vaikka se ei ole yhteensopiva vahvojen happojen kanssa. Se luokitellaan ärsyttäväksi aineeksi ja sen vaaroista voimme korostaa:
Se syövyttää silmiä (ne aiheuttavat sarveiskalvon vaurioita tai sokeutta) ja ihoa (ne aiheuttavat tulehdusta ja rakkuloita).
Pölyn hengittäminen aiheuttaa ärsytystä ruoansulatuskanavassa tai hengitysteissä, jolle on ominaista polttaminen, aivastelu ja yskä. Vaikea ylivalotus voi aiheuttaa keuhkovaurion, tukehtumisen, tajuttomuuden tai kuoleman. Silmän tulehdukseen on tunnusomaista punoitus, ärsytys ja kutina (Materiaaliturvallisuustiedote Kalsiumhydroksidi, 2013).
Toistuva altistuminen silmille alhaisella pölytasolla voi aiheuttaa ärsytystä ja paikallista ihon tuhoutumista tai ihon ihotulehdusta. Toistuva pölyn hengittäminen voi aiheuttaa vaihtelevan hengitysteiden ärsytyksen tai keuhkovaurion.
Jos tämä kemikaali joutuu kosketuksiin silmien kanssa, ne on pestävä välittömästi suurilla määrillä vettä, jolloin ajoittain nostettava ala- ja ylä silmäluomet. Välitön lääkärin hoito on saatava. Piilolinssejä ei tule käyttää tämän kemikaalin kanssa.
Jos tämä kemikaali joutuu iholle, saippualla ja vedellä saastunut iho on huuhdeltava välittömästi. Jos tämä kemikaali tunkeutuu vaatteisiin, poista vaatteet välittömästi ja huuhtele iho vedellä. Jos ärsytys jatkuu pesun jälkeen, hakeudu lääkärin hoitoon.
Jos suuria määriä tätä kemikaalia hengitetään, altistunut henkilö on siirrettävä raittiiseen ilmaan välittömästi. Jos hengitys on pysähtynyt, suorita suu-suu-elvytys, pitäen uhri lämpimänä ja levossa. Hakeudu lääkärin hoitoon mahdollisimman pian.
Jos ainetta on nielty, hakeuduttava välittömästi lääkärin hoitoon ja mahdollisuuksien mukaan näytettävä astia tai etiketti (kalsiumhydroksidimyrkytys, 2017).
Käsittely ja varastointi
- Yhdiste tulee säilyttää kuivassa säiliössä.
- Älä ime tai hengitä pölyä.
- Vettä ei saa koskaan lisätä tähän tuotteeseen.
- Jos ilmanvaihto on puutteellista, tuo riittävästi hengityslaitteita.
- Vältä aineen joutumista iholle ja silmiin.
- Pidä poissa epäyhteensopivista hapoista.
- Pidä säiliö tiiviisti suljettuna.
- Säilytä astia viileässä ja hyvin ilmastoidussa paikassa. Älä säilytä yli 25 astetta.
Käyttö ja sovellukset

Kalsiumhydroksidia tuotetaan suuressa mittakaavassa, sitä on helppo käsitellä ja se on yleensä halpaa, joten on monia merkittäviä käyttötarkoituksia ja sovelluksia.
Kalsiumhydroksidin merkittävä käyttö on kuin flokkulantti veden ja jäteveden käsittelyssä. Se muodostaa pehmeän ladatun kiinteän aineen, joka auttaa poistamaan pienempiä hiukkasia vedestä, mikä johtaa kevyempään tuotteeseen.
Tätä sovellusta mahdollistavat kalsiumhydroksidin alhaiset kustannukset ja alhainen myrkyllisyys. Sitä käytetään myös makean veden käsittelyyn veden pH: n nostamiseksi. Tarkoituksena on, että putket eivät syövy, jos pohjavesi on hapan.
Toinen suuri sovellus on paperiteollisuudessa, jossa sitä käytetään natriumhydroksidin tuotannossa. Tämä muuntaminen on osa tunnetun kraft-prosessia, jota käytetään massan uuttamisessa.
Elämää tukevissa järjestelmissä, kuten hiilidioksidipesureissa, erityisesti suljetun piirin sukellusreimulaattoreissa, joissa litiumhydroksidia, joka on kaustisempi, pidetään liian riskialtisena.
Sitä käytetään valkaisun ja rappauksen ainesosana niin sanottujen kalkkikiven avulla. Tienrakentamisessa kalsiumhydroksidi parantaa maaperän laatua.
Kansallisten terveyslaitosten mukaan kalsiumhydroksidia käytetään yleisesti hammaslääketieteessä antimikrobisena aineena, ja se on valinnainen aine muodostaen suojakerroksen, joka tunnetaan apikaalisina esteinä..
Apikaalisia esteitä käytetään yleisesti keinona välttää pulpulinkroosia tilanteissa, joissa endodontinen leikkaus olisi erityisen vaikeaa, mikä on yleensä seurausta epäkypsästä pysyvästä hampaasta..
Koska kalsiumhydroksidi voi auttaa desinfioimaan hampaita, jos infektio on jo olemassa, sitä voidaan käyttää lyhytaikaisena hoitona kivun ja tulehduksen vähentämiseksi valmisteltaessa endodontista leikkausta (Gottfried Schmalz, 2009).
Se toimii meriveden lisäaineena, koska se vähentää ilmakehän hiilidioksidia ja vähentää kasvihuoneilmiötä.
Metallien valmistuksessa kalkkia ruiskutetaan jätekaasuvirtaan happojen, kuten fluoridien ja kloridien, neutraloimiseksi ennen päästämistä ilmakehään..
Kalsiumhydroksidia käytetään aktiivisena emäksisenä ainesosana joissakin hiusten rentoutumisaineissa.
Cornell Center for Materials Researchin mukaan kalsiumhydroksidi voi suoristaa karheat hiukset, koska se rikkoo kysteiinejä yhdistäviä disulfidisidoksia, aminohappoja, jotka ovat läsnä korkeammissa pitoisuuksissa luonnostaan kiharat hiukset. Näiden sidosten rikkominen ja niiden tiivistäminen kalsiumhydroksidilla muuttaa pysyvästi käsiteltyjen hiusten fyysistä rakennetta.
Bordeaux-seoksessa kalsiumhydroksidi neutraloi liuoksen ja muodostaa pitkäaikaisen fungisidin.
Sitä käytetään öljynjalostusteollisuudessa öljyn lisäaineiden (salisylaatit, sulfitit, fenolit) valmistamiseksi petrokemian teollisuudessa eri tuotemerkkien kiinteän öljyn valmistukseen sekä kemianteollisuudessa kalsiumstearaatin valmistukseen. . Sitä käytetään yleisesti hiilidioksidin ja kaasun imeytymisen tutkimiseen.
Kalsiumhydroksidia käytetään jarrupalojen valmistuksessa, kuivien seosten valmistuksessa maalaukseen ja koristeluun sekä torjunta-aineiden seosten valmistukseen..
Sitä käytetään myös kalsiumlisänä ja pH / karbonaattipuskurina riutta-akvaarioiden korallinviljelyyn.
Se on "vaihtoehtoinen" luonnollinen hyönteismyrkky, suurin osa indeksoivista hyönteisistä, joka kuolee koskettamalla sitä, mukaan lukien punkit, kirput, kovakuoriaiset ja toukat (Russiver, 2015).
Kalsiumhydroksidi on tehokas ratkaisu hiusten erottamiseksi eläinten nahoista valmistettaessa nahkaa.
Kalsiumhydroksidin ja lämpimän veden seos muodostaa kylvyn, jossa tuoreita nahkoja on liotettava neljän päivän ajan ja ravisteltava usein. Tämä prosessi vapauttaa hiukset ja ihon niin paljon, että se voidaan yleensä poistaa käsin.
Vähäisen myrkyllisyytensä ja perusominaisuuksiensa pehmeyden vuoksi ravistettua kalkkia käytetään laajasti elintarviketeollisuudessa:
- Sokeriteollisuuden raakamehun ja sokerijuurikkaan raakamehun selvittäminen, alkoholijuomien ja virvoitusjuomien, suolakurkkojen ja muiden elintarvikkeiden prosessivesi.
- Tee maissitortilloja (auta maissijauhoa). Kalkilla keitetty maissi muunnetaan nixtamaliksi, mikä lisää merkittävästi niasiinin hyötyosuutta, sitä pidetään myös maukkaampana ja helpommin sulavaa.
- Puhdista kalsium- ja magnesiumkarbonaattien suolaliuos suolan valmistuksessa elintarvikkeiden ja lääkkeiden käyttöön.
- Vahvista hedelmäjuomia, kuten appelsiinimehua ja äidinmaidonkorviketta (BAUM, 2013).
viittaukset
- BAUM, J. (2013, 16. elokuuta). Kalsiumhydroksidikäyttö. Haettu osoitteesta livestrong.com: livestrong.com.
- Kalsiumhydroksidi Kaava - Kalsiumhydroksidin käyttö, ominaisuudet, rakenne ja kaava. (2005-2017). Haettu osoitteesta softschools.com.
- Kalsiumhydroksidimyrkytys. (2017, 7. helmikuuta). Haettu medlineplus.govista.
- Kemiallinen Datalehdet CALCIUM HYDROXIDE. (S.F.). Haettu osoitteesta cameochemicals.noaa.gov.
- Gottfried Schmalz, D. A. (2009). Hammasmateriaalien biologinen yhteensopivuus. Berliini: springer.
- Materiaaliturvallisuustiedote Kalsiumhydroksidi. (2013, 21. toukokuuta). Haettu osoitteesta sciencelab: sciencelab.com.
- Kansallinen bioteknologian tiedotuskeskus. (S.F.). PubChem-yhdistelmätietokanta; CID = 6093208. Haettu osoitteesta pubchem.ncbi.nlm.nih.gov.
- Royal Society of Chemistry. (2015). Kalsiumhydroksidi. Haettu osoitteesta ChemSpider: chemspider.com.
- Russiver, M. (2015, elokuu 17). Mikä on kalsiumhydroksidi? Haettu osoitteesta quora: quora.com.


