Vedettömät ominaisuudet, niiden muodostus, nimikkeistö, sovellukset
anhydridit ne ovat kemiallisia yhdisteitä, jotka ovat peräisin kahden molekyylin liitoksesta veden vapauttamisen kautta. Siten sitä voitaisiin pitää alkuaineiden kuivumisena; vaikka se ei ole aivan totta.
Orgaanisessa ja epäorgaanisessa kemiassa mainitaan niistä, ja molemmissa haaroissa ymmärrys eroaa huomattavasti. Esimerkiksi epäorgaanisessa kemiassa emäksisiä ja happamia oksideja pidetään vastaavasti niiden hydroksidien ja happojen anhydridinä, koska entinen reagoi veden kanssa muodostaakseen jälkimmäisen..

Tällöin sekaannukset voivat syntyä ilmaisujen "vedetön" ja "anhydridi" välillä. Yleensä vedetön tarkoittaa yhdistettä, joka on dehydratoitu ilman kemiallisen luonteen muutoksia (ei reaktiota); kun taas anhydridillä on kemiallinen muutos, joka heijastuu molekyylirakenteeseen.
Jos hydroksideja ja happoja verrataan niiden vastaaviin oksideihin (tai anhydrideihin), havaitaan, että reaktio oli olemassa. Sitä vastoin jotkut oksidit tai suolat voivat olla hydratoituja, menettää vettä ja pysyä samoina yhdisteinä; mutta ilman vettä, eli vedetöntä.
Orgaanisessa kemiassa toisaalta anhydridillä tarkoitetaan alkuperäistä määritelmää. Esimerkiksi yksi tunnetuimmista anhydrideistä on karboksyylihappojen johdannaiset (ylempi kuva). Nämä koostuvat kahden asyyliryhmän (-RCO) liitoksesta happiatomin avulla.
Sen yleisessä rakenteessa on esitetty R1 asyyliryhmälle ja R2 toisen asyyliryhmän osalta. Koska R1 ja R2 ne ovat erilaisia, ne ovat peräisin erilaisista karboksyylihapoista ja ovat sitten asymmetrinen happoanhydridi. Kun molemmat R-substituentit (riippumatta siitä, ovatko ne aromaattisia) ovat samoja, puhumme tässä tapauksessa symmetrisestä happoanhydridistä..
Kun yhdistetään kaksi karboksyylihappoa anhydridin muodostamiseksi, vesi voi muodostua tai olla muodostamatta, sekä muita yhdisteitä. Kaikki riippuu mainittujen happojen rakenteesta.
indeksi
- 1 Anhydridien ominaisuudet
- 1.1 Kemialliset reaktiot
- 2 Miten muodostuu anhydridit?
- 2.1 Sykliset anhydridit
- 3 Nimikkeistö
- 4 Sovellukset
- 4.1 Orgaaniset anhydridit
- 5 Esimerkkejä
- 5.1 Meripihkahappoanhydridi
- 5.2 Glutaarihappoanhydridi
- 6 Viitteet
Anhydridien ominaisuudet
Anhydridien ominaisuudet riippuvat siitä, mitä tarkoitat. Lähes kaikilla on yhteistä, että ne reagoivat veden kanssa. Niinpä epäorgaanisissa ns. Emäksisissä anhydridissä tosiasiallisesti useat niistä ovat jopa liukenemattomia veteen (MgO), joten tämä väite keskittyy karboksyylihappojen anhydrideihin.
Sulamis- ja kiehumispisteet putoavat (RCO): n molekyylirakenteeseen ja molekyylien välisiin vuorovaikutuksiin.2Tai tämä on näiden orgaanisten yhdisteiden yleinen kemiallinen kaava.
Jos molekyylipaino (RCO)2Tai se on alhainen, se on todennäköisesti väritön neste huoneenlämpötilassa ja paineessa. Esimerkiksi etikkahappoanhydridiä (tai etaanihappoanhydridiä), (CH3CO)2Tai se on nestemäistä ja teollisuudeltaan suurempaa nestettä ja sen tuotanto on erittäin suuri.
Etikkahappoanhydridin ja veden välistä reaktiota edustaa seuraava kemiallinen yhtälö:
(CH3CO)2O + H2O => 2CH3COOH
Huomaa, että kun vesimolekyyliä lisätään, vapautuu kaksi molekyyliä etikkahappoa. Käänteinen reaktio ei kuitenkaan voi esiintyä etikkahapolla:
2CH3COOH => (CH3CO)2O + H2O (Se ei tapahdu)
On tarpeen käyttää toista synteettistä reittiä. Dikarboksyylihapot voivat sitä vastoin kuumentaa; mutta se selitetään seuraavassa osassa.
Kemialliset reaktiot
hydrolyysi
Yksi anhydridien yksinkertaisimmista reaktioista on niiden hydrolyysi, joka on juuri osoitettu etikkahappoanhydridille. Tämän esimerkin lisäksi meillä on rikkihappoanhydridi:
H2S2O7 + H2O <=> 2H2SW4
Tässä on epäorgaaninen happoanhydridi. Huomaa, että H2S2O7 (jota kutsutaan myös disulfurihapoksi), reaktio itsessään on palautuva, joten lämmitys H2SW4 Konsentraatti johtaa sen anhydridin muodostumiseen. Jos taas se on laimennettu H-liuos2SW4, SO vapautetaan3, rikkihappoanhydridiä.
esteröimällä
Happoanhydridit reagoivat alkoholien kanssa, pyridiinillä väliaineessa, jolloin saadaan esteri ja karboksyylihappo. Esimerkiksi etikkahappoanhydridin ja etanolin välinen reaktio otetaan huomioon:
(CH3CO)2O + CH3CH2OH => CH3CO2CH2CH3 + CH3COOH
Näin muodostuu etyyliesteri-etanoaatti, CH3CO2CH2CH3, ja etaanihappo (etikkahappo).
Käytännössä tapahtuu, että hydroksyyliryhmän vety on substituoitu asyyliryhmällä:
R1-OH => R1-OCOR2
Jos kyseessä on (CH3CO)2Tai asyyliryhmä on -COCH3. Siksi sanotaan, että OH-ryhmä kärsii asyloinnista. Asylointi ja esteröinti eivät kuitenkaan ole keskenään vaihdettavia käsitteitä; Asylointi voi tapahtua suoraan aromaattisessa renkaassa, joka tunnetaan nimellä Friedel-Crafts-asylaatio.
Siten alkoholit happoanhydridien läsnä ollessa esteröidään asyloinnilla.
Toisaalta vain yksi kahdesta asyyliryhmästä reagoi alkoholin kanssa, muut pysyvät vetyä muodostaen karboksyylihapon; että (CH3CO)2Tai se on etaanihappo.
amidaatiota
Happoanhydridit reagoivat ammoniakin tai amiinien kanssa (primaariset ja sekundääriset) amidien saamiseksi. Reaktio on hyvin samanlainen kuin juuri kuvattu esteröinti, mutta ROH korvataan amiinilla; esimerkiksi sekundaarinen amiini, R2NH.
Jälleen reaktio (CH3CO)2O ja dietyyliamiini, Et2NH:
(CH3CO)2O + 2Et2NH => CH3CONET2 + CH3COO-+NH2et2
Ja muodostuu dietyyliasetamidi, CH3CONET2, ja karboksyyli- ammoniumsuola, CH3COO-+NH2et2.
Vaikka yhtälö voi tuntua hieman vaikeasti ymmärrettävältä, riittää, kun havaitsemme, miten ryhmä -COCH3 korvaa Et: n H2NH muodostaa amidin:
et2NH => Et2NCOCH3
Enemmän kuin amidaatiota reaktio on edelleen asylointi. Kaikki on tiivistetty tähän sanaan; tällä kertaa amiini kärsii asyloinnista eikä alkoholista.
Miten anhydridit muodostuvat?
Epäorgaaniset anhydridit muodostetaan saattamalla elementti reagoimaan hapen kanssa. Siten, jos elementti on metallista, muodostuu emäksinen metallioksidi tai anhydridi; ja jos se on ei-metallinen, muodostuu ei-metallinen oksidi tai happoanhydridi.
Orgaanisten anhydridien tapauksessa reaktio on erilainen. Kaksi karboksyylihappoa ei voi sitoutua suoraan veden vapauttamiseen ja muodostaa happoanhydridin; vaaditaan yhdisteen, jota ei ole vielä mainittu, osallistumista: asyylikloridi, RCOCl.
Karboksyylihappo reagoi asyylikloridin kanssa, jolloin saadaan vastaava anhydridi ja kloorivety:
R1COCl + R2COOH => (R1CO) O (COR2) + HCl
CH3COCl + CH3COOH => (CH3CO)2O + HCl
A CH3 tulee asetyyliryhmästä, CH3CO, ja toinen on jo läsnä etikkahapossa. Spesifisen asyylikloridin ja karboksyylihapon valinta voi johtaa symmetrisen tai asymmetrisen happoanhydridin synteesiin..
Sykliset anhydridit
Toisin kuin muut karboksyylihapot, jotka vaativat asyylikloridia, dikarboksyylihapot voidaan kondensoida vastaavassa anhydridissään. Tätä varten on tarpeen lämmittää ne H: n vapautumisen edistämiseksi2Esimerkiksi ftaalihappoanhydridin muodostuminen ftaalihaposta on esitetty.

Huomaa, kuinka viisikulmainen rengas on valmis, ja molemmat ryhmät C = O sitova happi on osa sitä; Tämä on syklinen anhydridi. Voidaan myös nähdä, että ftaalihappoanhydridi on symmetrinen anhydridi, koska molemmat R1 kuten R2 Ne ovat identtisiä: aromaattinen rengas.
Kaikki dikarboksyylihapot eivät kykene muodostamaan anhydridiä, koska kun niiden COOH-ryhmät on erotettu laajasti, niiden on pakko suorittaa suurempia ja suurempia renkaita. Suurin muodostettava rengas on kuusikulmainen, suurempi kuin reaktio ei tapahdu.
nimistö
Miten anhydridit nimetään? Kun jätetään pois oksidien kannalta epäorgaaniset aineet, tähän mennessä selitetyt orgaanisten anhydridien nimet riippuvat R: n identiteetistä.1 ja R2; toisin sanoen sen asyyliryhmistä.
Jos molemmat R: t ovat samat, riittää, että sana "happo" korvataan karboksyylihapon vastaavassa nimessä "anhydridiksi". Ja jos päinvastoin, nämä kaksi R: ää ovat erilaisia, ne on nimetty aakkosjärjestyksessä. Sen vuoksi, jotta voisimme tietää, mitä sitä kutsutaan, täytyy ensin nähdä, onko se symmetrinen tai asymmetrinen happoanhydridi.
(CH3CO)2Tai se on symmetrinen, koska R1= R2 = CH3. Etikka- tai etaanihapon johdannainen, joten sen nimi on edellisen selityksen mukaisesti: etikkahappoanhydridi tai etanohappo. Sama koskee juuri mainittua ftaalihappoanhydridiä.
Oletetaan, että sinulla on seuraava anhydridi:
CH3CO (O) COCH2CH2CH2CH2CH2CH3
Vasemmalla oleva asetyyliryhmä tulee etikkahaposta ja oikealla oleva heptanohappo. Tämän anhydridin nimeämiseksi sinun on nimettävä R-ryhmät aakkosjärjestyksessä. Niinpä sen nimi on: heptanohappoanhydridi.
sovellukset
Epäorgaanisilla anhydrideillä on loputon määrä sovelluksia, materiaalien, keramiikan, katalyyttien, sementtien, elektrodien, lannoitteiden jne. Synteesistä ja formuloinnista maankuoren päällystykseen tuhansilla rauta- ja alumiinimineraaleilla sekä dioksidilla. elävien organismien uloshengittämästä hiilestä.
Ne edustavat lähdön lähteenä, jossa monet epäorgaanisessa synteesissä käytetyt yhdisteet ovat peräisin. Yksi tärkeimmistä anhydridistä on hiilidioksidi, CO2. Se on yhdessä veden kanssa välttämätön fotosynteesille. Ja teollisuuden tasolla väitetiedoksianto3 se on ensiarvoisen tärkeää, koska vastaaja saa siitä rikkihappoa.
Ehkä anhydridiä, jossa on enemmän sovelluksia ja jolla on (niin kauan kuin on elämää) on yksi fosforihaposta: adenosiinitrifosfaatista, joka tunnetaan paremmin nimellä ATP, ja joka esiintyy DNA: ssa ja "energinen valuutta" aineenvaihdunnassa.
Orgaaniset anhydridit
Happoanhydridit reagoivat asyloimalla joko alkoholiin, joka muodostaa esterin, amiiniksi, joka saa aikaan amidin tai aromaattisen renkaan.
Jokaisesta näistä yhdisteistä on miljoonia, ja satoja tuhansia karboksyylihappovaihtoehtoja anhydridin valmistamiseksi; siksi synteettiset mahdollisuudet kasvavat voimakkaasti.
Täten yksi pääsovelluksista on asyyliryhmän sisällyttäminen yhdisteeseen, joka korvaa jonkin sen rakenteen atomeista tai ryhmistä.
Jokaisella erillisellä anhydridillä on omat sovelluksensa, mutta yleisesti ottaen ne kaikki reagoivat samalla tavalla. Tästä syystä näitä tyyppisiä yhdisteitä käytetään polymeerirakenteiden modifioimiseen, jolloin syntyy uusia polymeerejä; eli kopolymeerit, hartsit, pinnoitteet jne..
Esimerkiksi etikkahappoanhydridiä käytetään kaikkien selluloosan OH-ryhmien asetyloimiseksi (alempi kuva). Tällä tavoin kukin OH: n H korvataan asetyyliryhmällä COCH3.
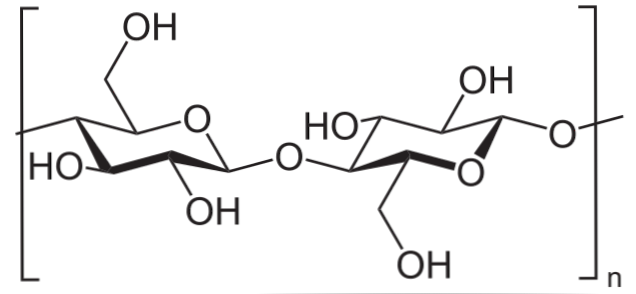
Tällä tavalla saadaan selluloosa-asetaattipolymeeri. Sama reaktio voidaan piirrää muiden polymeerirakenteiden kanssa NH-ryhmillä2, myös alttiita asyloinnille.
Nämä asylointireaktiot ovat käyttökelpoisia myös lääkkeiden, kuten aspiriinin (happo) synteesissä asetyylisalisyylihappoa).
esimerkit
Joitakin muita esimerkkejä orgaanisista anhydrideistä on esitetty loppuun. Vaikka niistä ei mainita, happiatomeja voidaan korvata rikki, jolloin saadaan rikkiä tai jopa fosforianhydridejä.
-C6H5CO (O) COC6H5: bentsoehappoanhydridi. Ryhmä C6H5 on bentseenirengas. Sen hydrolyysi tuottaa kaksi bentsoehappoa.
-HCO (O) COH: muurahaishappoanhydridi. Sen hydrolyysi tuottaa kaksi muurahaishappoa.
- C6H5CO (O) COCH2CH3: bentsoehaponihappoanhydridi. Sen hydrolyysi tuottaa bentsoehappoja ja propaanihappoja.
-C6H11CO (O) COC6H11: sykloheksaanikarboksyylihappoanhydridi. Toisin kuin aromaattiset renkaat, nämä ovat tyydyttyneet ilman kaksoissidoksia.
-CH3CH2CH2CO (O) COCH2CH3: butaanihaponanhydridi.
Meripihkahappoanhydridi

Tässä on toinen syklinen, joka on peräisin meripihkahaposta, dikarboksyylihapposta. Huomaa, kuinka kolme happiatomia pettävät tämän tyyppisen yhdisteen kemiallisen luonteen.
Maleiinihappoanhydridi on hyvin samankaltainen kuin meripihkahappoanhydridi, sillä erotuksella, että hiilen välillä on kaksoissidos, joka muodostaa viisikulmion pohjan..
Glutaarihappoanhydridi
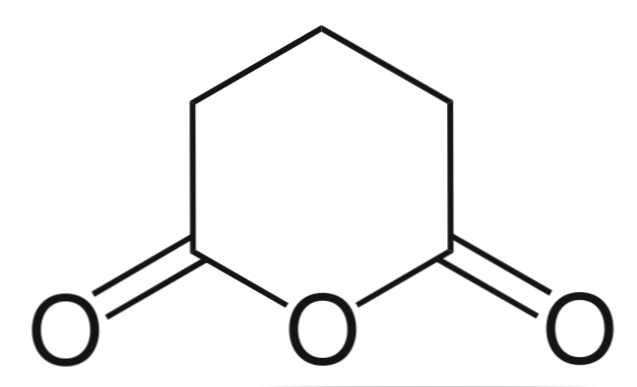
Lopuksi esitetään glutaarihapon anhydridi. Tämä rakenteellisesti erottuu kaikista muista muodostamalla kuusikulmainen rengas. Jälleen kolme happiatomia erottuvat rakenteesta.
Muita anhydridejä, monimutkaisempia, voi aina osoittaa kolme happiatomia, jotka ovat hyvin lähellä toisiaan.
viittaukset
- Encyclopaedia Britannican toimittajat. (2019). Anhydridi. Encryclopaedia Britannica. Haettu osoitteesta: britannica.com
- Helmenstine, Anne Marie, Ph.D. (8. tammikuuta 2019). Happoanhydridimääritys kemiassa. Haettu osoitteesta thinkco.com
- Kemia LibreTexts. (N.D.). Anhydridit. Haettu osoitteesta: chem.libretexts.org
- Graham Solomons T.W., Craig B. Fryhle. (2011). Orgaaninen kemia. Amiineja. (10th painos.). Wiley Plus.
- Carey F. (2008). Orgaaninen kemia (Kuudes painos). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Kemia. (8. painos). CENGAGE Learning.
- Morrison ja Boyd. (1987). Orgaaninen kemia (Viides painos). Addison-Wesley Iberoamericana.
- Wikipedia. (2019). Orgaanisen hapon anhydridi. Haettu osoitteesta: en.wikipedia.org


