Gram-värjäys, materiaalit, tekniikka ja käyttötarkoitukset
Gram-värjäys on yksinkertaisin ja hyödyllisin värjäysmenetelmä diagnostisessa mikrobiologiassa. Tämän tekniikan on luonut tanskalainen lääkäri Hans Christian Gram vuonna 1884, joka onnistui luokittelemaan bakteerit grampositiivisiksi ja gram-negatiivisiksi soluseinän koostumuksen mukaan.
Tekniikka muutti Huckerin tiettyjä muutoksia vuonna 1921 reagenssien stabiloimiseksi ja tahran laadun parantamiseksi siten, että Gram-värjäys tunnetaan myös nimellä Gram-Hucker.
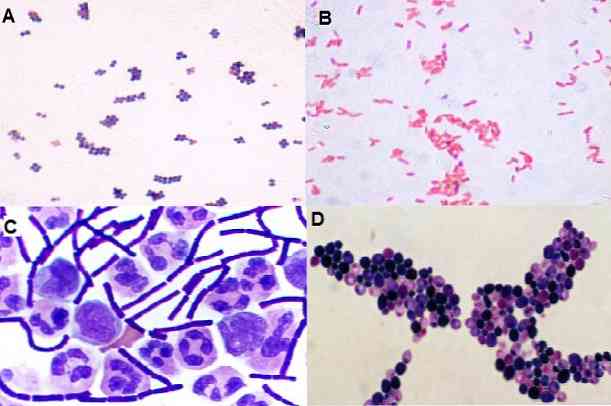
Tällä tekniikalla on myös mahdollista tarkkailla mikro-organismien muotoa, toisin sanoen, ovatko ne kokkeja, bacilloja, kokkobakteereja, pleomorfisia, filamentteja. Sen jakautuminen avaruudessa: klusterissa, ketjussa, eristyksissä, pareittain, tetradeina jne..
Kun epäillään bakteeri-infektiota, suurin osa vastaanotetuista näytteistä on levitettävä liukumaan ja värjätään grammalla tutkittavaksi mikroskoopin alla..
Gramin raportti ohjaa lääkäriä siitä, minkä tyyppinen mikro-organismi voi olla infektion aiheuttaja, ennen kuin saat lopullisen tuloksen.
Joissakin tapauksissa potilaan elämä on hyvin vaarantunut, joten lääkärit tarvitsevat pikaisesti Gramin raportin empiirisen hoidon aikaansaamiseksi odottaessaan mikro-organismin tunnistamista..
Esimerkiksi jos grammi paljastaa, että aivo-selkäydinnesteessä on grampositiivisia kokkeja, lääkäri suuntaa alkuperäisen hoidon antibiooteilla, jotka eliminoivat tämäntyyppisiä bakteereja, sille määrättyjen protokollien mukaisesti..
Kun lopullinen tulos saapuu eristetyn mikro-organismin ja sen vastaavan antibiootin nimellä, lääkäri arvioi, vaihdetaanko hoitoa vai ei. Tämä päätös tehdään tutkimuksen mukaan mikro-organismin alttiudesta antibiooteille, joita se vastaanottaa, ja potilaan kehittymisestä..
indeksi
- 1 Säätiö
- 2 Materiaalit
- 3 Väriaineiden ja reagenssien valmistus
- 3.1 Kristalliviolettiliuos
- 3.2 Jodo-Lugol
- 3.3 Valkaisu
- 3.4 Kontrasti
- 4 Reagenssien varastointi
- 5 Värillisen näytteen leviämisen valmistelu
- 5,1-suorien näytteiden gramma
- 5.2 - Viljelykehä
- 6 Tekniikka
- 7 Apuohjelma
- 8 Yleiset virheet
- 9 Viitteet
perusta
Tämä on tekniikka, jossa esitetään neljä perusvaihetta: värjäys, kiinnitys mordantin kanssa, värinmuutos ja kontraktio. Siksi tämä tekniikka bakteerien värjäämisen lisäksi erottaa ne.
Kristallivioletti on ensimmäinen käytetty väriaine. Siinä on affiniteetti peptidoglykaanille ja violetti värjättää kaikki läsnä olevat bakteerit, sitten asetetaan holkki, joka toimii mordanttina, eli se indusoi liukenemattomien kristalliviolijodi-ribonukleaaristen proteiinien kompleksien solussa.
Gram-positiiviset bakteerit, joilla on paksu peptidoglykaaniseinä, muodostavat enemmän komplekseja (kristallivioletijodi), joten ne säilyttävät väriaineen.
Se vaikuttaa myös siihen, että Gram-positiiviset bakteeriseinät sisältävät enemmän tyydyttymättömiä happoja, jotka osoittavat suurta affiniteettia hapettaville aineille (Lugol).
Samaan aikaan gramnegatiivisilla bakteereilla on ohut peptidoglykaanikerros, mikä tekee bakteereista vähemmän monimutkaisia kuin grampositiiviset bakteerit.
Sitten tulee vaiheen värinmuutos, jossa grampositiiviset ja gramnegatiiviset bakteerit käyttäytyvät eri tavalla.
Gramnegatiiviset bakteerit sisältävät ulomman kalvon, jossa on runsaasti lipopolysakkarideja ja joka on osa sen soluseinää. Rasvat tuhoutuvat joutuessaan kosketuksiin alkoholiasetonin kanssa, joten ulompi kalvo on epävakaa, violetti kristalli vapautuu.
Siten sitä värjätään sitten safraniinilla tai perusfuksiinilla, kun väri on punainen.
Gram-positiivisten bakteerien tapauksessa ne vastustavat värinmuutosta, koska valkaisuainetta suljetaan huokoset, mikä estää kristallivioletti- / jodikompleksin pääsyn.
Siksi violetti kristallin väri on vakaa, eikä safraniinille tai fuksiinille ole tilaa. Tämän vuoksi nämä bakteerit tahraavat voimakkaan sinisen tai violetin.
tarvikkeet
Gram-värityssarja koostuu:
- Violetti kristalli
- Lugolin
- Asetonialkoholi
- Safraniini tai perusfuksiini
Väriaineiden ja reagenssien valmistus
Kristalliviolettiliuos
Ratkaisu A:
Violetti kristalli -2 gr
Etyylialkoholi 95% -20cc
Ratkaisu B:
Ammoniumoksalaatti -0,8 g
Tislattu vesi -80 cm3
Violetinkiteiden lopullisessa valmistuksessa 1:10-liuos tulisi laimentaa tislatulla vedellä ja sekoitetaan 4 osaan liuosta B. Seosta säilytetään 24 tuntia ennen käyttöä. Se suodatetaan kolvissa, jossa on keltainen värjäys paperisuodattimella.
Päivittäin käytettävä määrä siirretään keltaiseen pulloon, jossa on tiputinta.
Jodi-Lugolin
Punnitaan ja mitataan kunkin yhdisteen ilmoitettu määrä seuraavasti:
Kiteet Iodo - 1gr
Kaliumjodidi - 2gr
Tislattu vesi -300 cm3
Kaliumjodidi liukenee vähitellen vedessä ja sitten lisätään jodi. Liuos ajetaan kullanväriseen pulloon.
Päivittäin käytettävä määrä siirretään pienempään keltaiseen pulloon, jossa on tiputinta.
valkaisu
95% etyylialkoholia -50 ml
Asetoni - 50 ml
Se on valmistettu yhtä suurina osina. Peitä hyvin, se pyrkii haihtumaan.
Aseta pulloon tippa.
Tämä valmiste antaa värinmuutoksen kohtuullisessa ajassa 5-10 sekuntia ja on suositeltavin.
Aloittelijat haluavat käyttää vain 95-prosenttista etyylialkoholia, jossa värinmuutos on hitaampi 10: stä 30: een sekuntiin.
Vaikka kokeneimmat voivat käyttää puhdasta asetonia, jossa värjäytyminen tapahtuu hyvin nopeasti 1 - 5 sekunnissa.
kontrasti
Safraniinivarastoliuos
Safranina -2,5 gr
Etyylialkoholi 95% -100 cm3
Kun punnitaan, ilmoitettu safraniinimäärä liukenee 100 ml: aan etyylialkoholia 95%: iin..
Käytettävä safraniiniliuos valmistetaan kantaliuoksesta.
Tätä varten mitataan 10 cm3 kantaliuosta, lisätään 90 ml tislattua vettä 100 ml: n valmistamiseksi.
On suositeltavaa siirtää määrä, jota käytetään päivittäin, keltaiseen pulloon pudottimella.
Mikro-organismit, jotka tahraavat heikosti Gram-negatiivisia Gram-Huckerin tahra, kuten tietyt anaerobit, Legionella sp, Campylobacter sp ja Brucella sp, ne voidaan värjätä paljon paremmin, jos käytetään Kopeloffin Gram-Huckerin värjäykseen tekemää modifikaatiota, nimeltään Gram-Kopeloff-värjäys,.
Tämä tekniikka muuttaa safraniiniväriä perusfuksiinilla. Tämän modifikaation avulla on mahdollista tehokkaasti värittää edellä mainitut mikro-organismit.
Reagenssien varastointi
Valmistetut väriaineet on säilytettävä huoneenlämmössä.
Näytteen valmistus levisi väreihin
Näytteen on oltava vähintään 105 mikro-organismit ennen mikro-organismin havainnointia tiskissä on todennäköistä. Levyt voidaan valmistaa suorasta näytteestä tai viljelmistä kiinteässä tai nestemäisessä väliaineessa.
Levitysten tulisi olla tasalaatuisia, hyvin jakautuneita eikä liian paksuja, jotta olemassa olevat rakenteet voidaan visualisoida paremmin.
-Suorien näytteiden gramma
Virtsan gramma ilman sentrifugia
Virtsa sekoitetaan ja 10 µl asetetaan liukumaan. Vähintään yhden bakteerin / upotuskentän havainto osoittaa, että infektio on olemassa.
Tämä tarkoittaa, että viljelmässä on noin yli 100 000 CFU / ml (105 CFU / ml) virtsan 85%: ssa tapauksista.
Tämä menetelmä ei ole käyttökelpoinen alle 100 000 CFU: n pesäkkeiden lukumäärässä.
LCR Gram
CSF on sentrifugoitava, supernatantti poistettava ja pelletti levitettävä liukumaan. Tämä neste on steriili normaaleissa olosuhteissa; bakteerien havainnointi osoittaa infektion.
Grammia hengityselimiä
Kudos Gram, keuhkoputkien tai keuhkoputkien huuhtelu, vaikkakin voi esiintyä erilaisia mikro-organismeja, ohjaa aina diagnoosissa, ja lisäksi se on hyödyllinen havaittujen solujen tyyppi..
Sputumin tapauksessa seos on valmistettava näytteen kaikkein kurjaimmilla osilla.
Stool Gram
Ei ole suositeltavaa suorittaa Gramia tämäntyyppisille näytteille, koska sillä ei ole diagnostista arvoa.
-Gramkasvit
Ne voidaan tehdä kahdella tavalla: yksi nestemäisistä kasveista ja toinen kiinteistä kasveista.
Nestemäiset kasvit
Nestemäisistä viljelmistä se on erittäin yksinkertaista; kevyempien lohkojen alle otetaan useita samean lihan paistoja ja ne asetetaan puhtaaseen ja kuivaan liukuun, joka antaa pyöreät liikkeet keskeltä kohti kehää, jotta materiaali jakautuu tasaisesti.
Sen annetaan kuivua itsestään ilmassa. Kuivumisen jälkeen materiaali kiinnitetään levylle lämmöllä. Tätä varten arkki 3 johdetaan puristimen avulla 4 kertaa Bunsen-polttimen liekin läpi varoen, ettei materiaalia polteta.
Levyn annetaan jäähtyä ja laittaa värityssillalle.
Kiinteät viljelmät
Voit suorittaa Gram-värin laajennuksen kiinteästä kulttuurista seuraavasti:
Ennen kuin valitset otettavia pesäkkeitä, liukukappale on valmistettava, ja se saattaa kaksi tippaa noin steriiliä fysiologista suolaliuosta.
Jos alkuperäinen viljelylevy sisältää useita eri tyyppisiä pesäkkeitä, valitaan jokainen yksittäinen pesäkkeestä Gramin suorittamiseksi. Jokainen pesäke otetaan platina-silmukalla sen liuottamiseksi suolaliuokseen, joka on aiemmin asetettu liukumaan.
Pyöreitä liikkeitä annetaan keskeltä kehälle, jotta siirtomaa jakautuu tasaisesti liukumaan..
Sen annetaan kuivua itsestään ilmassa. Kuivumisen jälkeen arkki kiinnitetään lämmöllä, kuten edellä on selitetty (liu'uttamalla liukuriviä kevyemmällä), varoen, ettet polta materiaalia.
Tämä toimenpide on suoritettava kullekin eri tyyppiselle pesäkkeelle. Paperiosassa on huomioitava havaitun järjestyksen, esimerkiksi:
Colony 1: Keltainen beeta-hemolyyttinen siirtomaa: Gram-positiivisia kookkeja havaittiin klustereissa
Colony 2: Cream colony, ilman hemolyysiä: havaittiin gramnegatiivisia kokkobasillija.
Jokainen arkki on merkittävä, jotta tiedämme, mitä tarkkaamme.
tekniikka
Gram-värjäysmenetelmä on erittäin helppo suorittaa ja suhteellisen edullinen, eikä sitä voida jättää huomiotta mikrobiologian laboratoriossa.
Sama tapahtuu seuraavasti:
- Kiinnitä lika lämpöön ja aseta värillinen silta.
- Levy peitetään kokonaan violetilla lasilla 1 minuutti.
- Pese vedellä. Älä kuivaa
- Peitä levy Lugol-liuoksella, jätä 1 minuutti. Pese vedellä. Älä kuivaa.
- Sekoita 5-10 sekuntia kevyesti sekoittaen asetonialkoholiin. Tai sijoita arkki pystyasentoon ja pudota pisaroita värinpoistoaineeseen pinnalle, kunnes jäljellä oleva violetti lasi vedetään pois. Älä ylitä.
- Pese vedellä. Älä kuivaa.
- Vaihtaminen arkki sillan väri ja kansi 30 sekuntia safranin (Gram-Hucker) tai 1 min perusfuksiinilla (gram-Kopeloff).
- Pese vedellä
- Anna kuivua itsestään pystysuorassa ilmassa.
Kun kuiva on asetettu, laita 1 pisara upotusöljyä sen tarkkailemiseksi optisessa mikroskoopissa tavoitteen 100X mukaisesti.
hyödyllisyys
Tämä tekniikka mahdollistaa eron useimpien bakteerien morfotyyppisistä eroista.
Hiivat erottuvat myös tällä värillä. He ottavat kristallivioletin, eli ne värjättävät Gram-positiivisia.
Lisäksi voidaan erottaa gram-positiivisia itiöitä muodostava, jossa vapaa tila sisällä basilli jossa sisäitiöitä muodostettu, vaikka itiöt eivät tahraa hyvin havaita. Muita tekniikoita värjäystä itiöiden käytetään Shaeffer-Fulton.
On huomattava, että tämä tahra ei ole tarkoitettu kaikenlaisten bakteerien värjäämiseen, toisin sanoen on tapauksia, joissa värjäys ei toimi.
Tässä tapauksessa voidaan mainita bakteerit, joissa ei ole soluseinää. Esimerkiksi: Mycoplasma-suku, sferoplastit, Ureaplasma, L-muodot ja protoplastit.
Lisäksi se värjää huonosti bakteereja runsaasti seinät mykolihappoja, kuten mykobakteerit ja solunsisäiset bakteerit Chlamydia ja Rickettsiae kuten.
Se on myös tehotonta useimpien spirochetal-bakteerien tahraamiseksi.
On olemassa samaan sukuun kuuluvia bakteereja, joita voidaan havaita samassa näytteessä kuin Gram-positiivinen ja Gram-negatiivisena. Kun näin tapahtuu, sitä kutsutaan muuttuvaksi Gram-väriksi, joka voi johtua ravintoaineiden muutoksista, lämpötilasta, pH: sta tai elektrolyyttien pitoisuudesta..
Yleisiä virheitä
Valkaisu liikaa
Värjäytymisvaiheessa liioittelu voi aiheuttaa väärien gram-negatiivisten mikro-organismien havainnoinnin.
Älä odota riittävästi kuivumisaikaa upottamalla öljyä:
Tämä virhe aiheuttaa rasvaisten micellien muodostumisen, jotka vaikeuttavat läsnä olevien rakenteiden havaitsemista. Tämä tapahtuu, kun öljy liittyy vesimolekyyleihin, jotka ovat likaantumisessa.
Käännä reagenssien järjestys:
Tällainen virhe aiheuttaa Gram-negatiivisten bakteerien näyttämisen purppuran, eli väärän Gram-positiivisen.
Käytä vanhoja kasveja (kiinteitä tai nestemäisiä):
Se voi aiheuttaa grampositiivisia bakteereita värjäämään Gram-negatiivisia (vääriä Gram-negatiivisia). Tämä johtuu siitä, että vanhoissa kulttuureissa on todennäköistä, että bakteereita on kuollut tai huonontunut, ja näissä olosuhteissa bakteerit eivät säilytä violettia kiteitä.
Käytä hyvin vanhaa Lugol-ratkaisua:
Ajan myötä tavarat menettävät ominaisuuksiaan ja sen väri heikkenee. Jos käytetään jo degeneroitunutta reagenssia, se ei kiinnitä kristalliviolettia hyvin, joten on mahdollista saada mikro-organismien visualisointi väärin Gram-negatiiviseksi.
Sinertävä tausta
Oikein värjäytynyt tausta on punainen. Sininen tausta osoittaa, että värinmuutos oli riittämätön.
viittaukset
- Ryan KJ, Ray C. 2010. Sherris. mikrobiologia Lääketieteellinen, 6. painos McGraw-Hill, New York, USA
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Mikrobiologinen diagnoosi. (5. painos). Argentiina, toimittaja Panamericana S.A..
- Forbes B, Sahm D, Weissfeld A. 2009. Bailey & Scottin mikrobiologinen diagnoosi. 12 toim. Argentiinassa. Panamericana S.A Toimituksellinen
- Casas-Rincón G. 1994. Yleinen mykologia. 2nd Ed. Universidad Central de Venezuela, kirjastoversiot. Venezuela, Caracas.
- "Gram tahra" Wikipedia, vapaa tietosanakirja. 4. lokakuuta 2018, 23:40 UTC. 9. joulukuuta 2018, 17:11. Otettu osoitteesta es.wikipedia.org.
- González M, González N. 2011. Lääketieteellisen mikrobiologian käsikirja. Toinen painos, Venezuela: Carabobon yliopiston tiedotusvälineiden ja julkaisujen osasto.
- López-Jácome L, Hernández-Durán M, Colín-Castro C, Ortega-Peña S, Cerón-González G, Franco-Cendejas F. Perusvärjäys mikrobiologian laboratoriossa. Tutkimus vammaisuudesta. 2014; 3 (1): 10-18.


