Proteinaasi K -ominaisuudet, entsymaattinen aktiivisuus ja sovellukset
proteinaasi K on entsyymi, joka kuuluu seriiniproteaasien ryhmään, toisin sanoen sen aktiivisessa katalyyttikeskuksessa on aminohapposeriini ja sen tehtävänä on hajottaa peptidisidokset hydrolyysillä. Tämä entsyymi puolestaan kuuluu proteiinien subtilisiinien (peptidaasi S8) perheeseen.
Proteinaasi K: n molekyylipaino (MW) on 28 900 daltonia ja se eristettiin ensimmäistä kertaa vuonna 1974 sienen uutteista Engyodontium-albumi, aiemmin tunnettu nimellä Tritirachium-albumi Limber.
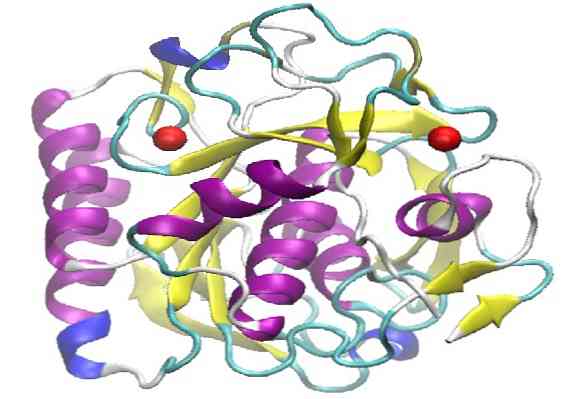
Siinä on korkea proteolyyttinen kapasiteetti, osoitettu pystyvän hajottamaan hiuksissa esiintyvän keratiinin. Sana keratiini Englanti on kirjoitettu "keratiini", joten sitä on kutsuttu "proteinaasi K".
Koska tämä entsyymi kykenee pilkkomaan natiivia proteiineja, se on käyttökelpoinen erilaisissa molekyylibiologian tekniikoissa. Sitä käytetään pääasiassa eristämään ja valmistamaan nukleiinihappoja, joilla on suuri molekyylipaino (MW).
Proteinaasi K toimii vapauttamalla ydin-DNA, samalla kun tuhoaa proteiinit ja inaktivoi RNaasit ja DNaasit, eli eliminoi nukleaasit DNA- ja RNA-valmisteissa..
Toisaalta on havaittu, että proteinaasi K voi hydrolysoida joitakin denaturoituja luonnollisia proteiineja, jotka ovat herättäneet tutkijoiden kiinnostusta sen käyttöön prioniproteiinien tutkimuksessa (PrPC).
Kuitenkin, vaikka proteolyyttinen teho on korkea, on proteiineja, jotka ovat resistenttejä proteinaasin K vaikutukselle. Näistä on joitakin epänormaaleja proteiineja, joita kutsutaan prioneiksi (PrPSc) ja jotka liittyvät tarttuviin spongiformisiin enkefalopatioihin.
indeksi
- 1 Proteinaasi K: n ominaisuudet
- 2 Entsyymiaktiivisuus
- 3 Sovellukset
- 4 Proteinaasi K: n edut
- 5 Proteinaasiresistentit proteiinit K
- 6 Viitteet
Proteinaasi K: n ominaisuudet
Proteinaasi K: lla on kolmikerroksinen muodostettu tertiäärinen rakenne, jossa on seitsemän ketjun p-arkki kahden helik- sierikerroksen väliin. Koska se kuuluu S8-peptidaasien perheeseen, sille on tunnusomaista, että sen aktiivisessa kohdassa on katalyyttinen triad, jonka peräkkäinen järjestys on (Asp, His ja Ser), joka erottaa ne muista peptidaasiperheistä..
Tämä entsyymi seriiniproteaasien ryhmästä on tunnettu siitä, että hydrolysoidaan peptidisidokset lähellä alifaattisten ja aromaattisten aminohappojen karboksyyliryhmää.
Toisaalta se kykenee toimimaan tiettyjen syövyttävien aineiden, kuten natriumdodekyylisulfaatin (SDS), Tris-HCL: n ja EDTA: n läsnä ollessa, joita käytetään proteiinien denaturoitumisen edistämiseen, jolloin ne menettävät natiivin rakenteensa.
Tämä on alustava vaihe proteiinien valmistuksessa elektroforeesitekniikkaa varten. PH-alue, jolla proteinaasi K toimii, on melko leveä (2,0 - 12,0), optimaalisen pH: n ollessa 7,5 - 12,0, ja sen isoelektrinen piste on 8,9. Kuten voidaan havaita, se on aktiivinen hyvin laajalla pH-alueella.
Toinen ominaisuus, joka erottuu proteinaasi K: sta, on sen stabiilisuus korkeiden lämpötilojen (50 - 60 ° C) läsnä ollessa..
Entsymaattinen aktiivisuus
Proteinaasi K tarvitsee kalsiumionin, vaikka se ei vaikuta sen aktiivisuuteen, jos on välttämätöntä säilyttää sen stabiilisuus.
Jotta proteinaasi K suorittaisi substraatin täydellisen pilkkomisen, tarvitaan noin 5 minuutin ja 2 tunnin välistä kosketusaikaa..
Tässä mielessä Daza et ai. Verrattuna useiden kerran proteinaasi K: n altistumiseen saadun DNA: n puhtautta ja totesi, että pitkäaikainen inkubointi (korkeintaan 24 h) parantaa merkittävästi DNA: n laatua..
Nyt, suhteessa proteiinin K-entsyymin eri pitoisuuksiin, voidaan sanoa, että se on hyvin vaihteleva.
Sitä voidaan käyttää hyvin pienistä pitoisuuksista (5 μg / ml) pitoisuuksiin 500 μg / ml. Yleisin työpitoisuus vaihtelee kuitenkin välillä 50-100 μg / ml, erityisesti proteiinien pilkkomisessa ja nukleaasien inaktivoitumisessa. Vaikka kudoshoitoon tarvitaan 2 mg / ml.
sovellukset
Sen sovellukset ovat hyvin laajoja, ja ne voidaan tiivistää seuraavasti:
-Sitä käytetään proteiinien pilkkomisessa ja DNA: n uuttamisessa useilla menetelmillä, kuten suolanpoistolla, PK-SDS: llä, setyyli-trimetyyliammoniumbromidilla (CTAB), modifioidulla kaliumasetaatilla ja uuttamisella natriumjodidilla..
-Nukleaasien inaktivointi (RNaasit ja DNaasit).
-Hybridisaatiotekniikassa in situ (HIS) nukleiinihapon vapauttamiseksi ei-toivottujen proteiinien eliminoinnin lisäksi.
-Proteiinimuutos.
-Tutkimustasolla eri tutkimuksissa.
Proteiini K: n edut
Proteinaasi K: ta käyttävissä DNA-uuttotekniikoissa on tehty useita vertailevia tutkimuksia muiden kanssa, jotka eivät käytä sitä, ja kaikki johtavat siihen, että entsyymiä käytettäessä on suurempia etuja. Eduista voidaan mainita seuraavat:
-Saadaan korkean molekyylipainon omaavaa DNA: ta, jolla on korkea laatu ja puhtaus.
-Uutettu DNA on stabiili jopa 3 kuukautta.
Uutettua DNA: ta voidaan käyttää seuraavissa tekniikoissa: Southern blot, polymeraasiketjureaktio (PCR), elektroforeesi, muun muassa.
Proteiinit K: lle vastustuskykyiset proteiinit
Eri tutkimukset ovat johtaneet siihen, että prionit (poikkeavat PrPSc-myrkylliset proteiinit) erotetaan PrPC-proteiineista (natiivit), koska ne ovat resistenttejä proteinaasi K: n vaikutuksesta, kun taas PrPC ovat herkkiä niiden vaikutukselle.
Muut tekijät ovat kuvailleet, että PrPSc: n rakenteessa on herkkiä osia ja muita proteinaasi K: lle resistenttejä. Molemmat osat ovat kuitenkin yhtä myrkyllisiä ja tarttuvia..
Toisaalta Bastian ja yhteistyökumppanit vuonna 1987 eristivät neljä proteiinia, jotka olivat 28, 30, 66 ja 76 kda. Spiroplasma mirum. Kaikki olivat vastustuskykyisiä proteinaasi K: n vaikutukselle, ja niillä oli myös ristireaktio joidenkin prionien kanssa.
On tunnettua, että tämä laji voi aiheuttaa kataraktia ja tärkeitä neurologisia vaurioita, ja koska Bastianin tieteellisten havaintojen mukaan muiden tutkimusten yhteydessä on yritetty yhdistää tämä mikro-organismi tarttuviin spongiformisiin enkefalopatioihin.
Tämän degeneratiivisen neurologisen patologian etiologia kuuluu kuitenkin edelleen prioneille tänään.
Tässä mielessä Butler ja yhteistyökumppanit vuonna 1991 tunnistivat ja karakterisoivat luokan 40 Kda-proteinaasiresistentin proteiinin K kahdesta kannasta. Mycoplasma hyorhinis. Tämä patogeeni vaikuttaa sioihin, jotka tarttuvat kudoksiin, mutta tässä tapauksessa ei ollut ristireaktiota testattujen prionien kanssa.
Tarvitaan lisää tutkimusta, jotta voidaan selvittää monia tuntemattomia.
viittaukset
- Bastian F, Jennings R ja Gardner W. 1987. Antiserumi scrapien kanssa liittyvälle fibriiliproteiinille reagoi ristiin Spiroplasma mirum fibriiliproteiineja. J. Clin. Microbiol. 25: 2430 - 2431.
- Daza C, Guillen J, kuningas J, Ruiz V. DNA: n uuttamis- ja puhdistusmenetelmän arviointi lihaskudoksesta, joka on kiinnitetty formaldehydiin tunnistamattomista kaavista. Med Magazine, 2014; 22 (1): 42-49,
- Butler G, Kotani H, Kong L, Frick M, Evancho S, Stanbridge E ja Mcgarrity G. Tunnistaminen ja karakterisointi proteinaasi-K-resistenteistä proteiineista luokan Mollikuuttien jäsenissä. Infection and Immunity, 1991, 59 (3): 1037-1042
- López M, Rivera M, Viettri M, Lares M, Morocoima A, Herrera L, et ai. Kahden DNA: n erottamisen protokollan vertailu Trypanosoma cruzi kasvatetaan aksiaalisessa väliaineessa. Peru. Med. Exp. Kansanterveys 2014; 31 (2): 222-227. Saatavilla osoitteessa: scielo.org
- Jiménez G, Villalobos M, Jiménez E ja Palma W. Parafiinimateriaalin viiden DNA-uuttamisprotokollan tehokkuuden määrittäminen molekulaarisissa tutkimuksissa. Rev Méd Univ Costa Rica. 2007; 1 (1): 10-19.


