Kultaoksidin (III) (Au2O3) rakenne, ominaisuudet, nimikkeistö ja käyttö
kultaoksidi (III) on epäorgaaninen yhdiste, jonka kemiallinen kaava on Au2O3. Teoreettisesti voidaan olettaa, että sen luonne on kovalenttinen. Tietyn ionisen merkin läsnäoloa sen kiinteässä aineessa ei kuitenkaan voida hylätä kokonaan; tai mikä on sama, olettaa, että ei ole olemassa toimilupaa3+ anionin O vieressä2-.
Voi tuntua ristiriitaiselta, että kulta, joka on jalometalli, voi ruostua. Normaaleissa olosuhteissa kultaa (kuten alla olevassa kuvassa olevat tähdet) ei voida hapettaa kosketuksella ilmakehän hapen kanssa; jos säteilytetään ultraviolettisäteilyllä otsonin läsnä ollessa, OR3, kuva on erilainen.

Jos kultaiset tähdet joutuisivat näihin olosuhteisiin, he kääntyisivät punaiselle ruskealle, Au: lle ominaiselle2O3.
Muita menetelmiä tämän oksidin saamiseksi edellyttäisi mainittujen tähtien kemiallista käsittelyä; esimerkiksi muuntamalla kullan massa vastaavaksi kloridiksi, AuCl: ksi3.
Jälkeen AuCl3, ja muut muodostuneet mahdolliset kultaiset suolat lisätään, voimakas emäksinen väliaine lisätään; ja näin saat hydratoidun oksidin tai hydroksidin, Au (OH)3. Lopuksi tämä viimeinen yhdiste dehydratoidaan termisesti Au: n saamiseksi2O3.
indeksi
- 1 Kultaoksidin rakenne (III)
- 1.1 Sähköiset näkökohdat
- 1.2 Hydraatit
- 2 Ominaisuudet
- 2.1 Fyysinen ulkonäkö
- 2.2 Molekyylipaino
- 2.3 Tiheys
- 2.4 Sulamispiste
- 2.5 Stabiilisuus
- 2.6 Liukoisuus
- 3 Nimikkeistö
- 4 Käyttö
- 4.1 Lasien väritys
- 4.2 Auraattien synteesi ja kultahitsaus
- 4.3 Itserakenteisten yksikerrosten käsittely
- 5 Viitteet
Kultaoksidin rakenne (III)
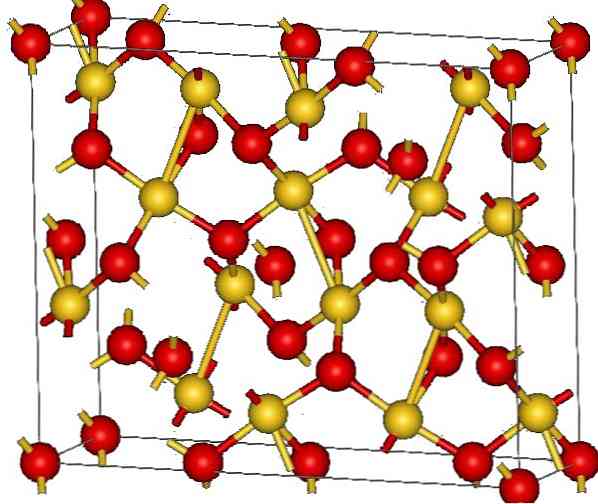
Kullan (III) oksidin kiderakenne on esitetty ylemmässä kuvassa. Kulta- ja happiatomien järjestely kiinteässä aineessa on esitetty joko neutraaleina atomina (kovalenttisena kiinteänä aineena) tai ioneina (ioninen kiinteä aine). Epäilemättä riittää, että poistetaan tai asetetaan Au-O-linkit joka tapauksessa.
Kuvan mukaan oletetaan, että kovalenttinen merkki on vallitseva (mikä olisi looginen). Tästä syystä esitetyt atomit ja sidokset esitetään vastaavasti palloilla ja palkeilla. Kultaiset pallot vastaavat kulta-atomeja (AuIII-O) ja punertavan tai hapen atomeja.
Jos tarkastelet huolellisesti, näet, että on olemassa AuO-yksiköitä4, jotka on liitetty happiatomeihin. Toinen tapa visualisoida olisi ajatella, että kukin Au3+ ympäröi neljä O2-; Tietenkin, ionisesta näkökulmasta.
Tämä rakenne on kiteinen, koska atomeja pyydetään noudattamaan samaa pitkän kantaman kuviota. Siten sen yhtenäinen solu vastaa rombohedraalista kiteistä järjestelmää (sama kuin ylemmässä kuvassa). Siksi kaikki Au2O3 voitaisiin rakentaa, jos kaikki yksikön solun alat jaetaan avaruuteen.
Elektroniset näkökohdat
Kulta on siirtymämetalli, ja on odotettavissa, että sen 5d-orbitaalit ovat vuorovaikutuksessa suoraan happiatomin 2p-orbitaalien kanssa. Näiden kiertoradojen päällekkäisyyksien pitäisi teoriassa tuottaa johtokuntia, jotka muuttavat Au: n2O3 kiinteässä puolijohteessa.
Siksi Au: n todellinen rakenne2O3 on entistä monimutkaisempi.
kosteuttaa
Kultaoksidi voi säilyttää vesimolekyylejä romboediakiteissään, mikä saa aikaan hydraatteja. Kun tällaisia hydraatteja muodostetaan, rakenne muuttuu amorfiseksi, ts.
Tällaisten hydraattien kemiallinen kaava voi olla mikä tahansa seuraavista, joita ei itse asiassa ole selvitetty syvästi: Au2O3∙ zH2O (z = 1, 2, 3 jne.), Au (OH)3, tai AuxOja(OH)z.
Kaava Au (OH)3 on mainittujen hydraattien todellisen koostumuksen ylikäsittely. Tämä johtuu siitä, että kullan hydroksidin (III) sisällä tutkijat ovat löytäneet myös Au: n2O3; ja siksi on järkevää käsitellä sitä erillisenä "yksinkertaisena" siirtymämetallihydroksidina.
Toisaalta kiinteää ainetta, jolla on kaava AuxOja(OH)z amorfista rakennetta voitaisiin odottaa; koska tämä riippuu kertoimista x, ja ja z, joiden vaihtelut johtaisivat kaikenlaiseen rakenteeseen, joka voisi tuskin osoittaa kiteistä kuviota.
ominaisuudet
Fyysinen ulkonäkö
Se on punertavanruskea kiinteä aine.
Molekyylipaino
441,93 g / mol.
tiheys
11,34 g / ml.
Sulamispiste
Se sulaa ja hajoaa 160 ºC: ssa. Siksi siinä ei ole kiehumispistettä, joten tämä oksidi ei koskaan saavuta kiehumispistettä.
pysyvyys
Au2O3 se on termodynaamisesti epävakaa, koska, kuten alussa mainittiin, kulta ei yleensä hapeta normaaleissa lämpötilaolosuhteissa. Joten se on helppo vähentää, jotta siitä tulee jälleen jalo kulta.
Mitä korkeampi lämpötila, sitä nopeammin reaktio, joka tunnetaan lämpö- hajoamisena. Joten, Au2O3 160 ° C: ssa se hajoaa tuottamaan metallista kultaa ja vapauttamaan molekyylin happea:
2 Au2O3 => 4 Au + 3 O2
Erittäin samanlainen reaktio voi tapahtua muiden yhdisteiden kanssa, jotka suosivat mainittua pelkistystä. Miksi vähentäminen? Koska kulta palaa saada elektronit, jotka happi otti pois siitä; joka on sama kuin sanomalla, että se menettää yhteyksiä happeen.
liukoisuus
Se on veteen liukenematon kiinteä aine. Se on kuitenkin liukoinen kloorivetyhappoon ja typpihappoon kulta- kloridien ja nitraattien muodostumisen vuoksi.
nimistö
Kultaoksidi (III) on nimikkeistön mukainen nimike. Muita tapoja mainita se on:
-Perinteinen nimikkeistö: aurerinen oksidi, koska valenssi 3+ on kultaa korkein.
-Järjestelmällinen nimikkeistö: dioro-trioksidi.
sovellukset
Lasien väritys
Yksi sen merkittävimmistä käyttötarkoituksista on tarjota tietyille materiaaleille, kuten lasille, punertavia värejä ja antaa tietyille kulta-atomeille ominaisia ominaisuuksia..
Auraattien synteesi ja kultahitsaus
Jos Au lisätään2O3 väliaineeseen, jossa se on liukoinen, ja metallien läsnä ollessa auraat voivat saostua vahvan emäksen lisäämisen jälkeen; jotka muodostavat AuO-anionit4- metallisten kationien yritys.
Myös Au2O3 reagoi ammoniakin kanssa muodostaen kullan fulminoivan yhdisteen, Au2O3(NH3)4. Sen nimi johtuu siitä, että se on erittäin räjähtävää.
Itse koottujen yksikerrosten käsittely
Kulta ja sen oksidi tietyt yhdisteet, kuten dialkyylidisulfidit, RSSR, eivät ole adsorboituneet samalla tavalla. Kun tämä adsorptio tapahtuu, muodostuu spontaanisti Au-S-sidos, jossa rikkiatomi osoittaa ja määrittelee mainitun pinnan kemialliset ominaisuudet sen funktionaalisen ryhmän mukaan, johon se on sitoutunut..
RSSR ei voi adsorboitua Au: lle2O3, mutta metallisella kullalla. Siksi, jos kultaa ja sen hapettumisastetta muutetaan, sekä Au: n hiukkasten tai kerrosten koko2O3, heterogeenisempi pinta voidaan suunnitella.
Tämä pinta Au2O3-AuSR on vuorovaikutuksessa tiettyjen elektronisten laitteiden metallioksidien kanssa.
viittaukset
- Wikipedia. (2018). Kulta (III) oksidi. Haettu osoitteesta: en.wikipedia.org
- Kemiallinen formulaatio (2018). Kultaoksidi (III). Palautettu osoitteesta: formacionquimica.com
- D. Michaud. (24. lokakuuta 2016). Kultaoksidit. 911 Metallurgi. Haettu osoitteesta: 911metallurgist.com
- Shi, R. Asahi ja C. Stampfl. (2007). Kultaoksidien Au ominaisuudet2O3 ja Au2O: Ensimmäisten periaatteiden tutkimus. American Physical Society.
- Cook, Kevin M. (2013). Kultaoksidi peitekerroksena regioselektiiviselle pintakemialle. Opinnäytteet ja väitöskirjat. Paperi 1460.


