Litiumoksidikaava, ominaisuudet, riskit ja käyttötavat
litiumoksidi on epäorgaaninen yhdiste, jolla on kaava Li2Tai joka on muodostettu yhdessä pienien määrien kanssa litiumperoksidia, kun litiummetallia poltetaan ilmassa ja yhdistetään happeen.
Metalli- ja litiummarkkinoita hallitsi 1990-luvulle saakka Yhdysvaltojen tuotanto mineraalivarastoista, mutta 2000-luvun alussa suurin osa tuotannosta oli peräisin muista kuin Yhdysvaltojen lähteistä; Australia, Chile ja Portugali olivat tärkeimmät toimittajat maailmassa. Boliviassa on puolet maailman litium-talletuksista, mutta se ei ole suuri tuottaja.
Tärkein kaupallinen muoto on litiumkarbonaatti, Li2CO3, valmistettu mineraalista tai suolavedestä useilla eri prosesseilla.
Kun litium poltetaan ilmassa, päätuote on litiumoksidin valkoinen liuos, Li2O. Lisäksi tuotetaan jonkin verran litiumperoksidia, Li2O2, myös valkoinen.
Se voidaan tehdä myös litiumhydroksidin, LiOH: n tai litiumperoksidin, Li2O2: n termisellä hajoamisella.
4Li (s) + O2(g) → 2Li2O (t)
2LiOH (t) + lämpö → Li2O (s) + H2O (g)
2Li2O2(s) + lämpö → 2Li2O (s) + O2(G)
Fysikaaliset ja kemialliset ominaisuudet
Litiumoksidi on valkoinen kiinteä aine, joka tunnetaan litiumina ja jolla ei ole aromia eikä suolaa. Sen ulkonäkö on esitetty kuvassa 2 (Kansallinen bioteknologian tiedotuskeskus, 2017).

Kuvio 2: litiumoksidin ulkonäkö
Litiumoksidi ovat kiteitä, joiden antifloriitti-geometria on samanlainen kuin natriumkloridin (kuutio keskitetty kasvoille). Sen kiteinen rakenne on esitetty kuvassa 3 (Mark Winter [Sheffieldin yliopisto ja WebElements Ltd, 2016].
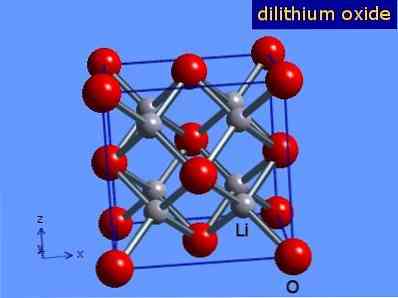
Kuvio 3: litiumoksidin kiteinen rakenne.
Sen molekyylipaino on 29,88 g / mol, sen tiheys on 2,013 g / ml ja sulamis- ja kiehumispisteet ovat vastaavasti 1438 ° C ja 2066 ° C. Yhdiste on hyvin liukoinen veteen, alkoholiin, eetteriin, pyridiiniin ja nitrobentseeniin (Royal Society of Chemistry, 2015).
Litiumoksidi reagoi helposti vesihöyryn kanssa, jolloin muodostuu hydroksidia, ja hiilidioksidilla muodostuu karbonaattia; Siksi se on varastoitava ja käsiteltävä puhtaassa ja kuivassa ilmakehässä.
Oksidiyhdisteet eivät johda sähköön. Jotkin perovskiitin rakenteelliset oksidit ovat kuitenkin elektronisia johtimia, jotka soveltuvat kiinteiden oksidien polttokennojen ja hapenmuodostusjärjestelmien katodiin..
Ne ovat yhdisteitä, jotka sisältävät ainakin yhden happianionin ja yhden metallikationin (American Elements, S.F.)..
Reaktiivisuus ja vaarat
Litiumoksidi on stabiili yhdiste, joka ei ole yhteensopiva vahvojen happojen, veden ja hiilidioksidin kanssa. Tiedämme, että litiumoksidin kemiallisia, fysikaalisia ja toksikologisia ominaisuuksia ei ole tutkittu ja raportoitu syvällisesti.
Litiumyhdisteiden toksisuus on niiden liukoisuuden veteen funktio. Litiumionilla on keskushermoston toksisuus. Yhdiste on erittäin syövyttävää ärsyttävää, jos se joutuu silmiin, ihoon hengitettynä tai nieltynä (ESPI METALS, 1993).
Jos silmät joutuvat kosketuksiin, tarkista, onko sinulla piilolinssejä ja poista ne välittömästi. Silmät on huuhdeltava juoksevalla vedellä vähintään 15 minuutin ajan pitäen silmäluomet auki. Voit käyttää kylmää vettä. Salvaa ei tule käyttää silmiin.
Jos kemikaali joutuu kosketuksiin vaatteiden kanssa, poista se mahdollisimman nopeasti ja suojaa omia käsiäsi ja kehoa. Aseta uhri turvallisen suihkun alle.
Jos kemikaali kerääntyy uhrin altistuneelle iholle, kuten kädet, pese juoksevalla vedellä ja ei-hankaavalla saippualla saastunut iho varovasti ja huolellisesti. Voit käyttää kylmää vettä. Jos ärsytys jatkuu, hakeudu lääkärin hoitoon. Pese saastunut vaatetus ennen uudelleenkäyttöä.
Jos hengitettynä, uhri saa antaa levätä hyvin ilmastoidussa tilassa. Jos hengitys on vakava, uhri on evakuoitava turvalliseen alueeseen mahdollisimman pian.
Löysää tiukat vaatteet, kuten paita kaulus, vyöt tai solmio. Jos uhri on vaikea hengittää, on annettava happea. Jos uhri ei hengitä, elvytetään suu-suuhun.
Aina ottaen huomioon, että apua antavan henkilön voi olla vaarallista antaa suuhun suuhun elvytystä, kun hengitettävä materiaali on myrkyllistä, tarttuvaa tai syövyttävää.
Kaikissa tapauksissa sinun on hakeuduttava välittömästi lääkärin hoitoon (SIGMA-ALDRICH, 2010).
sovellukset
Litiumoksidia käytetään keraamisten lasien vuoksena ja luo sinistä kuparia ja ruusuja koboltilla. Litiumoksidi reagoi veden ja höyryn kanssa muodostaen litiumhydroksidia ja se on eristettävä niistä.
Litiumoksidi (Li2O), jolla on korkea tritiumpotentiaali, on houkutteleva ehdokas DT-fuusiovoimalaitoksen kiinteälle viljelymateriaalille johtuen sen suuresta litiumatomien tiheydestä (verrattuna muihin litium- tai metalliseen litiumkeramiikkaan) ja sen johtokykyyn suhteellisen korkea lämpö (LITHIUM OXIDE (Li2O), SF).
li2Tai se altistuu korkeille lämpötiloille neutronien säteilytyksessä fuusiohujen käytön aikana. Näissä olosuhteissa Li: ssä esiintyy suuri määrä säteilytysvikoja2Tai kuten heliumin aiheuttama turvotus, suhteellisen korkea lämpölaajeneminen, viljan kasvu, LiOH: n (T) muodostuminen ja saostuminen alhaisissa lämpötiloissa ja LiOH (T) -massan kuljettaminen korkeissa lämpötiloissa.
Lisäksi Li2Tai se kohdistuu jännityksiin, jotka johtuvat Li-lämpölaajenemisen eroista2O ja rakennemateriaalit. Nämä Li: n ominaisuudet2Tai ne johtavat haastaviin teknisiin ongelmiin sekä huovan valmistuksessa että suunnittelussa.
Mahdollinen uusi käyttö on korvata kobolttia ja litiumoksidia katodina litiumioniakuissa, joita käytetään sähkölaitteiden käyttämiseen matkapuhelimista kannettaviin tietokoneisiin sekä akkukäyttöisiin autoihin (Reade International Corp, 2016).
viittaukset
- Mark Winter [Sheffieldin yliopisto ja WebElements Oy (2016). webelements. Otettu litiumista: dilithium oxide webelements.com.
- American Elements. (S.F.). Litiumoksidi. Takaisin americanelements americanelements.comista.
- ESPI METALS. (1993, kesäkuu). Litiumoksidi. Otettu espimetals espimetals.com.
- LITIUMOXIIDI (Li2O). (S.F.). Otettu ferp.ucsd.edu ferp.ucsd.edu.
- Kansallinen bioteknologian tiedotuskeskus. (2017, kesäkuu 24). PubChem-yhdistelmätietokanta; CID = 166630. Takaisin PubChem pubchem.ncbi.nlm.nih.gov.
- Reade International Corp. (2016). Litiumoksidijauhe (Li2O). Otettu osoitteesta reade.com
- Royal Society of Chemistry. (2015). Litiumoksidi.Otettu chemspiderchemspider.com-sivustosta.
- Sigma-Aldrich. (2010). Materiaaliturvallisuustiedote Litiumoksidi. Otettu chemblink chemblink.comista.


