Eksoterminen reaktio, tyypit ja esimerkit
eksoterminen reaktio on kemiallisen reaktion tyyppi, jossa tapahtuu energiasiirto, pääasiassa lämmön tai valon vapautumisen muodossa. Nimi tulee Kreikan etuliitteestä ekso, mikä tarkoittaa "ulkomailla"; ja termi "lämpö", joka viittaa lämpöön tai lämpötilaan.
Tässä mielessä eksotermiset reaktiot voivat siirtää muita energiamuotoja ympäristöön, jossa ne syntyvät, kuten räjähdykset ja niiden tapa siirtää kineettistä ja sonicenergiaa, kun aineita, jotka ovat kaasufaasissa korkeissa lämpötiloissa, laajennetaan. väkivaltaisesti.
Samoin myös paristojen käytössä suoritetaan eksoterminen reaktio, vain tässä tapauksessa sähköenergiaa kuljetetaan.
indeksi
- 1 Prosessi
- 2 tyyppiä
- 2.1 Palamisreaktiot
- 2.2 Neutralointireaktiot
- 2.3 Hapetusreaktiot
- 2.4 Termiittireaktio
- 2.5 Reaktiopolymerointi
- 2.6 Ydinfissio
- 2.7 Muut reaktiot
- 3 Esimerkkejä
- 4 Viitteet
prosessi
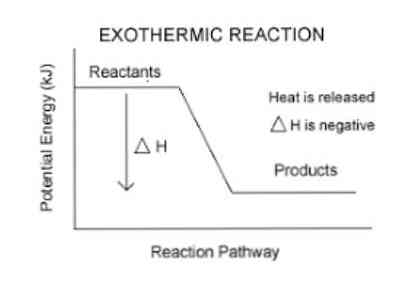
Aiemmin mainittiin, että kun eksoterminen reaktio tapahtuu, energia vapautuu, joka voidaan visualisoida helpommin seuraavassa yhtälössä:
Reagenssit → Tuotteet + Energia
Joten järjestelmän absorboiman tai vapautuneen energian kvantifioimiseksi käytetään termodynaamista parametria, jota kutsutaan entalpiaksi (merkitty "H"). Jos järjestelmässä (tässä tapauksessa kemiallinen reaktio) on energiaa vapautumassa ympäristöön, entalpian vaihtelu (ilmaistuna ΔH: na) on negatiivinen arvo.
Muussa tapauksessa, jos tämän mittauksen vaihtelu on positiivinen, se heijastaa lämmön imeytymistä ympäristöstä. Lisäksi järjestelmän entalpian variaation suuruus ilmaisee energian määrän, joka siirretään ympäristöön tai ympäristöön.
Mitä suurempi AH: n suuruus, sitä suurempi on energian vapautuminen järjestelmästä ympäröivään väliaineeseen.
Tämä johtuu siitä, että näissä reaktioissa uusien linkkien luomisessa vapautuva nettoenergia on suurempi kuin linkkien hajanaisuudessa käytetty nettoenergia..
Edellä esitetystä voidaan päätellä, että tällaiset reaktiot ovat hyvin yleisiä, koska reaktiotuotteissa on energiaa, joka on tallennettu sidoksiin, jotka ovat suurempia kuin mitä reagensseissa on..
tyyppi
Eri kemiallisilla aloilla on olemassa erilaisia eksotermisiä reaktioita, joko laboratoriossa tai teollisuudessa; jotkut toteutetaan spontaanisti ja toiset tarvitsevat erityisiä olosuhteita tai jonkinlaista ainetta, kuten tuotettavaa katalyyttiä.
Seuraavat ovat eksotermisten reaktioiden tärkeimmät tyypit:
Palamisreaktiot
Palamisreaktiot ovat redoksityyppisiä reaktioita, jotka ilmenevät, kun yksi tai useampi aine reagoi hapen kanssa, mikä yleensä johtaa valon ja lämpöenergian vapautumiseen eli valoon ja lämpöön, kun liekki tuotetaan..
Neutralointireaktiot
Neutralointireaktioille on tunnusomaista happolajin ja alkalisen aineen (emäksen) välinen vuorovaikutus suolan ja veden muodostamiseksi, joka ilmentää eksotermistä luonnetta.
Hapetusreaktiot
On olemassa monia tämän tyyppisiä reaktioita, jotka osoittavat eksotermisen käyttäytymisen, koska hapen hapettuminen aiheuttaa suuren määrän energiaa, kuten hiilivetyjen hapetuksessa..
Termiitti-reaktio
Tämä reaktio voi tuottaa noin 3000 ° C: n lämpötilan ja alumiinijauheen suuren affiniteetin ja suuren määrän metallioksideja johtuen sitä käytetään teräksen ja raudan hitsauksessa..
Polymerointireaktio
Tämäntyyppinen reaktio on sellainen, joka syntyy, kun tietty määrä kemiallisia aineita, joita kutsutaan monomeereiksi, reagoi, jotka ovat yksiköitä, jotka yhdistettynä toistetaan ketjuissa muodostamaan makromolekyylirakenteita, joita kutsutaan polymeereiksi.
Ydinfissio-reaktio
Tämä prosessi viittaa raskaaksi katsottavan atomin ytimen jakautumiseen, eli massanumeroon (A), joka on suurempi kuin 200, sellaisten fragmenttien tai ytimien tuottamiseksi, joiden koko on pienempi ja joiden välimassa on keskimääräinen massa.
Tässä reaktiossa, jossa muodostuu yksi tai useampi neutroni, vapautuu suuri määrä energiaa, koska ytimellä, jonka paino on suurempi, on alhaisempi stabiilisuus kuin sen tuotteet.
Muut reaktiot
On myös muita erittäin merkityksellisiä eksotermisiä reaktioita, kuten joidenkin hiilihydraattien dehydratoituminen, kun se reagoi rikkihapon kanssa, veden imeytyminen, jossa on natriumhydroksidia altistettuna ulkoilmaan, tai metallien hapettuminen monissa korroosio-reaktioissa.
esimerkit
Alla on muutamia esimerkkejä eksotermisistä reaktioista, jotka tuottavat entalpian vaihtelun, jolla on negatiivinen arvo, koska ne vapauttavat energiaa, kuten edellä mainittiin..
Esimerkiksi propaanin palaminen on spontaani eksoterminen reaktio:
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O (l)
Toinen eksotermisen käyttäytymisen tapaus osoitetaan natriumkarbonaatin ja suolahapon välisellä neutralointireaktiolla:
NaHCO3(ac) + HCI (ac) → NaCl (ac) + H2O (l) + CO2(G)
Esitetään myös etanolin hapettuminen etikkahappoon, jota käytetään hengityselimissä, jonka täydellinen reaktio on esitetty seuraavassa yhtälössä:
3CH3CH2OH + 2K2op2O7 + 8H2SW4 → CH3COOH + 2Cr (SO4)3 + 2K2SW4 + 11H2O
Toinen eksotermisen reaktion luokka on ns. Termiittireaktio, jossa alumiini yhdistetään metallioksidiin, kuten alla on esimerkinomaisesti esitetty:
2Al (t) + Usko2O3→ Al2O3(s) + Fe (l)
Edellä esitettyjen esimerkkien lisäksi on olemassa monia erilaisia reaktioita, joita pidetään myös eksotermisinä, kuten tiettyjen orgaanisten jätemateriaalien hajoaminen kompostointiin..
Siinä korostetaan myös lusiferiinipigmentin hapettumista lusiferaasin entsyymin vaikutuksesta, jotta saadaan aikaan monien muiden reaktioiden joukossa firefliesille ominainen bioluminesenssi ja jopa hengitys..
viittaukset
- Wikipedia. (N.D.). Eksoterminen reaktio. Haettu osoitteesta es.wikipedia.org
- BBC. (N.D.). Energian muutokset ja palautuvat reaktiot. Haettu osoitteesta bbc.co.uk
- Chang, R. (2007). Kemia, yhdeksäs painos. (McGraw-Hill).
- Walker, D. (2007). Kemialliset reaktiot. Haettu osoitteesta books.google.co.ve
- Saunders, N. (2007). Kemiallisten reaktioiden tutkiminen. Haettu osoitteesta books.google.co.ve


