Strontiumhydroksidi (Sr (OH) ₂) kemiallinen rakenne, ominaisuudet ja käyttötarkoitukset
strontiumhydroksidi (Sr (OH) ₂) on epäorgaaninen kemiallinen yhdiste, joka koostuu strontiumionista (Sr) ja kahdesta hydroksidi (OH) -ionista. Tämä yhdiste saadaan yhdistämällä strontsiumsuola vahvan emäksen kanssa, jolloin saadaan emäksistä yhdistettä, jonka kemiallinen kaava on Sr (OH)2.
Yleensä natriumhydroksidia (NaOH) tai kaliumhydroksidia (KOH) käytetään vahvana emäksenä strontiumhydroksidin valmistamiseksi. Toisaalta stronsiumsuola (tai strontiumioni), joka reagoi vahvan emäksen kanssa, on strontiumnitraatti Sr (NO3)2 ja prosessia kuvataan seuraavalla kemiallisella reaktiolla:
2KOH + Sr (NO3)2 → 2KNO3 + Sr (OH)2
Liuoksessa strontiumkationi (Sr+) saatetaan kosketukseen hydroksidianionin (OH) kanssa-) muodostavat strontiumin emäksisen ionisen suolan. Koska strontium on maa-alkalimetalli, strontiumhydroksidia pidetään emäksisenä alkaliseoksena.
indeksi
- 1 Hankkiminen
- 2 Kemiallinen rakenne ja fysikaalis-kemialliset ominaisuudet
- 2.1 Strontiumhydroksidioktahydraatti
- 2.2 Strontiumhydroksidimonohydraatti
- 2.3 Vedetön strontiumhydroksidi
- 2.4 Liukoisuus
- 2.5 Kemiallinen reaktiivisuus
- 3 Käyttö
- 3.1 Melassin uuttaminen ja sokerijuurikkaan jalostus
- 3.2 Strontiumrasvat
- 3.3 Muovinen stabilointiaine
- 3.4 Muut sovellukset
- 4 Viitteet
hankkiminen
Aiemmin selitetyn prosessin lisäksi voidaan sanoa, että kun reaktio on suoritettu, Sr (OH)2 saostuu liuokseen. Sitten se pestään ja kuivataan, jolloin saadaan lopuksi erittäin hieno valkoinen jauhe.
Vaihtoehtoinen menetelmä strontiumhydroksidin saamiseksi on strontiumkarbonaatin (SrCO) kuumentaminen.3) tai strontium-sulfaatti (SrSO)4) höyryllä lämpötilassa 500 ° C - 600 ° C. Kemiallinen reaktio tapahtuu seuraavasti:
SrCO3 + H2O → Sr (OH)2 + CO2
SrS + 2H2O → Sr (OH)2 + H2S
Kemiallinen rakenne ja fysikaalis-kemialliset ominaisuudet
Tällä hetkellä tunnetaan kolme strontiumhydroksidin muotoa: oktahydraatti, monohydraatti ja vedetön.
Strontiumhydroksidi-oktahydraatti
Liuoksista normaaleissa lämpötilan ja paineen olosuhteissa (25 ° C ja 1 atm) strontiumhydroksidi saostuu oktahydratoidussa muodossa, jonka kemiallinen kaava on Sr (OH)2∙ 8H2O.
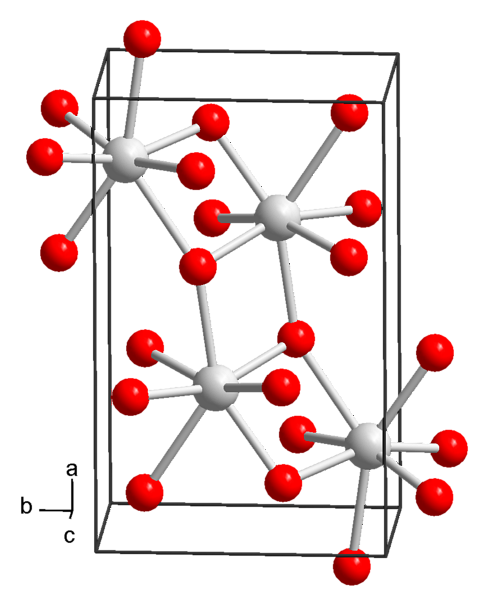
Tämän yhdisteen moolimassa on 265,76 g / mol, tiheys 1,90 g / cm ja saostuu nelikulmaisten kiteinä (tilaryhmällä P4 / ncc) nelikulmaisena ja värittömänä prismaattisena ulkonäönä.
Myös strontiumhydroksidioktahydraatilla on kyky imeä ilmakehän kosteutta, koska se on helposti haihtuva yhdiste.
Strontiumhydroksidimonohydraatti
Optisten mikroskooppisten tutkimusten mukaan (suoritetaan röntgendiffraktiotekniikalla) nostamalla lämpötila noin 210 ° C: een - vakiolämpötilassa - Sr (OH)2∙ 8H2Tai se dehydratoidaan ja transformoidaan strontiumhydroksidimonohydraatiksi (Sr (OH)2∙ H2O).
Tämän yhdisteen moolimassa on 139,65 g / mol ja sen sulamislämpötila on -73,15 ° C (375 K). Atomikokoonpanonsa ansiosta se liukenee veteen alhaisemmin kuin oktahydratoidussa muodossa.
Vedetön strontiumhydroksidi
Jatkamalla järjestelmän lämpötilan nostamista noin 480 ° C: seen dehydraatio jatkuu, kunnes saadaan vedetön strontiumhydroksidi..
Toisin kuin sen hydratoiduissa muodoissa, sen moolimassa on 121,63 g / mol ja tiheys 3,625 g / cm3. Sen kiehumispiste saavutetaan 710 ° C: ssa (1 310 ° F tai 983 K), kun taas sulamispiste on 535 ° C (995 ° F tai 808 K)..
liukoisuus
Strontiumin oktahydratoidun hydroksidin liukoisuus veteen on 0,91 grammaa 100 millilitraa kohden (mitattuna 0 ° C: ssa), kun taas sen vedettömän muodon liukoisuus samoissa lämpötilaolosuhteissa on 0,41 grammaa 100 millilitraa kohti..
Samalla tavalla tätä ainetta pidetään liukenematon asetoniin ja liukenee täysin happoihin ja ammoniumkloridiin.
Kemiallinen reaktiivisuus
Strontiumhydroksidi ei ole syttyvä, sen kemiallinen reaktiivisuus pysyy vakaana kohtuullisissa lämpötiloissa ja paineissa, ja se kykenee absorboimaan hiilidioksidia ilmakehän ilmasta muuttamalla sen strontiumkarbonaatiksi.
Lisäksi se on voimakkaasti ärsyttävä yhdiste, jos se joutuu kosketuksiin ihon, hengitysteiden tai muiden kehon limakalvojen kanssa..
sovellukset
Hygroskooppisten ominaisuuksiensa ja perusominaisuuksiensa vuoksi strontiumhydroksidia käytetään eri sovelluksiin teollisuudessa:
- Melassin uuttaminen ja sokerin jalostus juurikkaista.
- Muovinen stabilointiaine.
- Rasvat ja voiteluaineet.
Melassin uuttaminen ja sokerijuurikkaan jalostus
2000-luvun alussa Saksassa käytettiin strontiumhydroksidia sokerin jalostukseen sokerijuurikkaasta Carl Scheiblerin patentoimalla prosessilla vuonna 1882.
Tämä menetelmä käsittää strontiumhydroksidin ja juurikkaan sokerimassan sekoittamisen, mikä johtaa liukenemattomaan disakkaridiin. Tämä liuos erotetaan dekantoimalla ja kun jalostusprosessi on suoritettu, sokeri saadaan lopputuotteena.
Vaikka tätä menettelyä käytetään edelleen nykyään, on muitakin menetelmiä, joilla on paljon enemmän kysyntää, koska ne ovat halvempia, joita käytetään valtaosassa maailman sokeritehtaista. Esimerkiksi Barsil-menetelmä, jossa käytetään bariumsilikaattia tai terävöitymenetelmää käyttäen Calia uuttolaitteena.
Strontiumrasvat
Ne ovat voitelurasvoja, jotka sisältävät strontiumhydroksidia. Ne pystyvät tarttumaan voimakkaasti metalliominaisuuksille, kestävät vettä ja kestävät äkillisiä lämpötilan muutoksia.
Näiden rasvojen fyysisen ja kemiallisen stabiilisuuden vuoksi niitä käytetään teollisina voiteluaineina.
Muovinen stabilointiaine
Suurin osa muoveista, jotka altistuvat ilmasto-tekijöille, kuten auringolle, sateelle ja ilmakehän hapelle, muuttavat niiden ominaisuuksia ja hajoamista.
Koska vesipitoisuus on huomattava, näihin polymeereihin lisätään strontiumhydroksidia fuusio-vaiheen aikana, joka toimii stabilisaattorina muovituotteiden valmistuksessa niiden käyttöiän pidentämiseksi.
Muut sovellukset
- Maaliteollisuudessa sitä käytetään olennaisena lisäaineena kuivausprosessin nopeuttamiseksi kaupallisissa ja teollisissa maaleissa.
- Strontiumsuolat tai strontiumionit saadaan strontiumhydroksidista ja niitä käytetään raaka-aineena pyroteknisten tuotteiden valmistuksessa..
viittaukset
- Wikipedia. (N.D.). Strontiumhydroksidi. Haettu osoitteesta en.wikipedia.org
- Pubchem. (N.D.). Strontiumhydroksidi. Haettu osoitteesta pubchem.ncbi.nlm.nih.gov
- Lambert, I. ja Clever, H. L. (2013). Alkaliset maa-hydroksidit vedessä ja vesiliuoksissa. Haettu osoitteesta books.google.co.ve
- Krebs, R. E. (2006). Maamme kemiallisten elementtien historia ja käyttö: ohjekirja. Haettu osoitteesta books.google.co.ve
- Honeywell. (N.D.). Strontiumhydroksidi-oktahydraatti. Palautettu osoitteesta honeywell.com


