Berylliumhydroksidi (Be (OH) 2), kemiallinen rakenne, ominaisuudet ja käyttötarkoitukset
berylliumhydroksidi on kemiallinen yhdiste, joka koostuu kahdesta hydroksidimolekyylistä (OH) ja berylliumimolekyylistä (Be). Sen kemiallinen kaava on Be (OH)2 ja se on tunnettu siitä, että se on amfoteerinen laji. Yleensä se voidaan saada berylliummonoksidin ja veden välisestä reaktiosta seuraavan kemiallisen reaktion mukaisesti: BeO + H2O → Be (OH)2
Toisaalta tämän amfoteerisen aineen molekyylikokoonpano on lineaarinen. Beryliumhydroksidin eri rakenteita voidaan kuitenkin saada: alfa- ja beeta-muodossa, mineraalina ja höyryfaasina riippuen käytetystä menetelmästä.
indeksi
- 1 Kemiallinen rakenne
- 1.1 Berylliumhydroksidi alfa
- 1.2 Beta-beryylihydroksidi
- 1.3 Berylliumhydroksidi mineraaleissa
- 1.4 Berylliumhydroksidin höyry
- 2 Ominaisuudet
- 2.1 Ulkonäkö
- 2.2 Termokemialliset ominaisuudet
- 2.3 Liukoisuus
- 2.4 Altistumisesta johtuvat riskit
- 3 Käyttö
- 4 Hankkiminen
- 4.1 Metallisen berylliumin hankkiminen
- 5 Viitteet
Kemiallinen rakenne
Tämä kemiallinen yhdiste löytyy neljästä eri tavalla:
Berylliumhydroksidi alfa
Lisäämällä mitä tahansa emäksistä reagenssia, kuten natriumhydroksidia (NaOH) berylliumsuolaliuokseen, saadaan berylliumhydroksidin alfa (a) -muoto. Seuraavassa on esimerkki:
2NaOH (laimennettu) + BeCl2 → Be (OH)2↓ + 2NaCl
2NaOH (laimennettu) + BeSO4 → Be (OH)2↓ + Na2SW4
Beryllium-beta-hydroksidi
Tämän alfa-tuotteen rappeutuminen muodostaa stabiilin tetragonaalisen kristallirakenteen, joka on pitkäkestoisen ajan jälkeen muuttunut rombiseksi rakenteeksi, jota kutsutaan berylliumhydroksidibetaksi (β).
Tämä beetamuoto saadaan myös saostumana natriumberylliumin liuoksesta hydrolyysillä olosuhteissa, jotka ovat lähellä sulamispistettä.
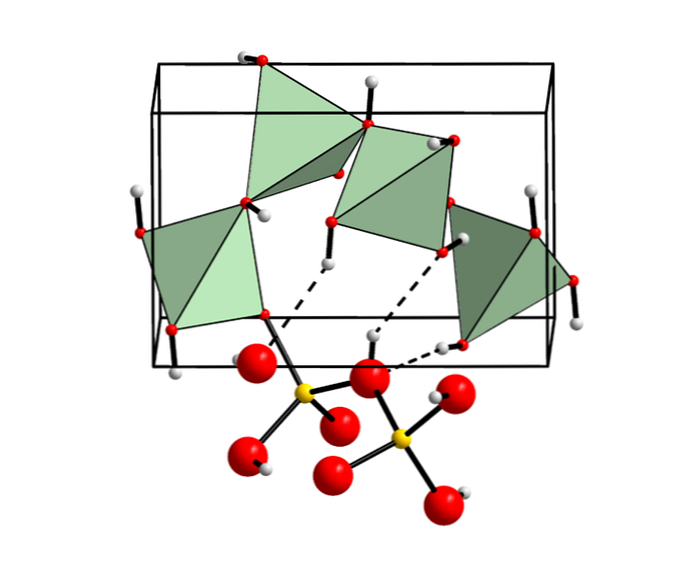
Berylliumhydroksidi mineraaleissa
Berylliumhydroksidia esiintyy kuitenkin kristallisena mineraalina, joka tunnetaan nimellä behoite (jota kutsutaan tällä tavalla sen kemiallisen koostumuksen perusteella)..
Sitä esiintyy graniittisissa pegmatiiteissa, jotka muodostuvat Gadoliniten (silikaattiryhmän mineraalit) muuttamisesta tulivuoren fumaroleissa..
Tämä suhteellisen uusi mineraali löydettiin ensimmäisen kerran vuonna 1964, ja se löytyy tällä hetkellä vain graniittipegmatiiteista, jotka sijaitsevat Texasissa ja Utahissa Yhdysvalloissa..
Berylliumhydroksidin höyry
Yli 1200 ° C: n (2190 ° C) lämpötiloissa berylliumhydroksidi on höyryfaasissa. Se saadaan vesihöyryn ja berylliumoksidin (BeO) välisestä reaktiosta..
Samoin tuloksena olevan höyryn osapaine on 73 Pa, mitattuna 1500 ° C: n lämpötilassa.
ominaisuudet
Beryliumhydroksidin moolimassa tai molekyylipaino on noin 43,0268 g / mol ja tiheys 1,92 g / cm.3. Sen sulamispiste on 1000 ° C: n lämpötilassa, jossa se alkaa hajoaa.
Mineraalina Be (OH)2 (behoita): n kovuus on 4 ja sen tiheys vaihtelee välillä 1,91 g / cm3 ja 1,93 g / cm3.
ulkomuoto
Beryliumhydroksidi on valkoinen kiinteä aine, jolla on alfa-muodossaan gelatiininen ja amorfinen ulkonäkö. Toisaalta tämän yhdisteen beetamuoto muodostuu hyvin määritellystä, ortorombisesta ja stabiilista kiteisestä rakenteesta.
Voidaan sanoa, että Be (OH) -mineraalin morfologia2 se vaihtelee, koska se löytyy retikulaarisista kiteistä, arborescent- tai pallomaisista aggregaateista. Samoin se on valkoinen, vaaleanpunainen, sinertävä ja jopa väritön ja rasvainen lasiainen kiilto.
Termokemialliset ominaisuudet
Muodostumisen entalpia: -902,5 kJ / mol
Gibbs-energia: -815,0 kJ / mol
Muodostumisen entropia: 45,5 J / mol
Lämpöteho: 62,1 J / mol
Ominaislämpökapasiteetti: 1 443 J / K
Muodostumisen vakio entalpia: -20,98 kJ / g
liukoisuus
Beryliumhydroksidi on luonteeltaan amfoteerinen, joten se kykenee luovuttamaan tai hyväksymään protoneja ja liukenee sekä happamia että emäksisiä väliaineita happo-emäsreaktiossa, jolloin saadaan suolaa ja vettä.
Tässä mielessä Be (OH): n liukoisuus2 vesiliukoisuus rajoittuu liukoisuustuotteella Kps(H2O), joka on 6,92 × 10-22.
Altistumisriskit
Berylliumhydroksidiaineen laillisesti sallittu altistumisraja (PEL tai OSHA), joka on määritelty suurimmaksi pitoisuudeksi 0,002 mg / m3 ja 0,005 mg / m3 on 8 tuntia ja konsentraation ollessa 0,0225 mg / m3 enintään 30 minuuttia.
Nämä rajoitukset johtuvat siitä, että beryllium luokitellaan syöpää aiheuttavaksi aineeksi tyyppi A1 (syöpää aiheuttava aine ihmisillä, epidemiologisissa tutkimuksissa saatujen todisteiden määrän perusteella)..
sovellukset
Beryliumhydroksidin käyttö raaka-aineena joidenkin tuotteiden käsittelyssä on hyvin rajallinen (ja epätavallinen). Se on kuitenkin yhdiste, jota käytetään pääasiallisena reagenssina muiden yhdisteiden synteesissä ja berylliummetallin saamisessa.
hankkiminen
Berylliumoksidi (BeO) on kemiallinen yhdiste, joka on erittäin puhdasta berylliumia, jota käytetään eniten teollisuudessa. Sille on ominaista väritön kiinteä aine, jolla on sähköeristysominaisuudet ja korkea lämmönjohtavuus.
Tässä mielessä prosessi sen synteesille (teknisesti) alkutuotannossa suoritetaan seuraavasti:
- Berylliumhydroksidi liuotetaan rikkihappoon (H2SW4).
- Kun reaktio suoritetaan, liuos suodatetaan siten, että liukenemattomat oksidin tai sulfaatin epäpuhtaudet poistetaan tällä tavalla..
- Suodos haihdutetaan tuotteen väkevöimiseksi, joka jäähdytetään berylliumsulfaatin BeSO kiteiden saamiseksi.4.
- BeSO4 kalsinoidaan tietyssä lämpötilassa välillä 1100 ° C ja 1400 ° C.
Lopputuotetta (BeO) käytetään teolliseen käyttöön tarkoitettujen erityisten keraamisten kappaleiden valmistukseen.
Metallisen berylliumin hankkiminen
Berylliumin mineraalien uuttamisen ja käsittelyn aikana syntyy epäpuhtauksia, kuten berylliumoksidia ja berylliumhydroksidia. Jälkimmäiselle suoritetaan useita muutoksia, kunnes saadaan metallinen beryllium.
Be (OH) reagoi2 ammoniumbifluoridiliuoksella:
Be (OH)2 + 2 (NH4) HF2 → (NH4)2BeF4 + 2 H2O
(NH4)2BeF4 se altistuu lämpötilan nousulle, jolla on terminen hajoaminen:
(NH4)2BeF4 → 2NH3 + 2HF + BeF2
Lopuksi beryliumfluoridin pelkistäminen 1300 ° C: n lämpötilassa magnesiumin (Mg) kanssa johtaa berylliummetalliin:
BeF2 + Mg → Be + MgF2
Berylliumia käytetään metalliseoksissa, elektronisten komponenttien valmistuksessa, säteilysuojien ja röntgenlaitteiden valmistuksessa.
viittaukset
- Wikipedia. (N.D.). Berylliumhydroksidi. Haettu osoitteesta en.wikipedia.org
- Holleman, A. F .; Wiberg, E. ja Wiberg, N. (2001). Berylliumhydroksidi. Haettu osoitteesta books.google.co.ve
- Julkaisu, M. D. (s.f.). Behoite. Haettu osoitteesta handbookofmineralogy.org
- Kaikki reaktiot. (N.D.). Berylliumhydroksidi Be (OH)2. Haettu osoitteesta allreactions.com
- Pubchem. (N.D.). Berylliumhydroksidi. Haettu osoitteesta pubchem.ncbi.nlm.nih.gov
- Walsh, K. A. ja Vidal, E. E. (2009). Beryllium-kemia ja käsittely. Haettu osoitteesta books.google.co.ve


