Kalsiumfosfaatti (Ca3 (PO4) 2) rakenne, ominaisuudet, muodostuminen ja käyttö
kalsiumfosfaatti on epäorgaaninen ja tertiäärinen suola, jonka kemiallinen kaava on Ca3(PO4)2. Kaava ilmoittaa, että tämän suolan koostumus on kalsium- ja fosfaattiosassa 3: 2. Tämä näkyy suoraan alemmassa kuvassa, jossa Ca-kationi näytetään2+ ja anionin PO43-. Jokaisesta kolmesta Ca: sta2+ PO on kaksi43- vuorovaikutuksessa heidän kanssaan.
Toisaalta kalsiumfosfaatti viittaa sarjaan suoloja, jotka vaihtelevat Ca / P-suhteen mukaan, samoin kuin hydraatio- ja pH-aste. Itse asiassa on olemassa monia erilaisia kalsiumfosfaatteja, joita on olemassa ja joita voidaan syntetisoida. Nimikkeistön mukaisesti kirjaimellisesti kalsiumfosfaatti viittaa vain edellä mainittuun trikalsiumiin.

Kaikki kalsiumfosfaatit, mukaan lukien Ca3(PO4)2, Ne ovat kiinteitä valkoisia, hieman harmaita sävyjä. Ne voivat olla rakeisia, hienojakoisia, kiteisiä ja niiden hiukkaskoko on noin mikrometriä; ja jopa näiden fosfaattien nanohiukkaset on valmistettu, joiden kanssa luodaan biologisesti yhteensopivia materiaaleja.
Tämä biologinen yhteensopivuus johtuu siitä, että nämä suolat löytyvät hampaista ja lyhyt- näisesti nisäkkäiden luukudoksista. Esimerkiksi hydroksiapatiitti on kiteinen kalsiumfosfaatti, joka vuorostaan vuorovaikutuksessa saman suolan amorfisen faasin kanssa.
Tämä tarkoittaa, että on olemassa amorfisia ja kiteisiä kalsiumfosfaatteja. Tästä syystä monimuotoisuus ja useat vaihtoehdot eivät ole yllättäviä, kun syntetisoidaan kalsiumfosfaatteihin perustuvia materiaaleja; materiaalit, joiden ominaisuuksista tutkijat ovat kiinnostuneempia päivittäin maailmanlaajuisesti keskittymään luiden palauttamiseen.
indeksi
- 1 Kalsiumfosfaatin rakenne
- 1.1 Amorfinen kalsiumfosfaatti
- 1.2 Loput perheestä
- 2 Fysikaaliset ja kemialliset ominaisuudet
- 2.1 Nimet
- 2.2 Molekyylipaino
- 2.3 Fyysinen kuvaus
- 2.4 Maku
- 2.5 Sulamispiste
- 2.6 Liukoisuus
- 2.7 Tiheys
- 2.8 Taitekerroin
- 2.9 Koulutuksen tavallinen entalpia
- 2.10 Säilytyslämpötila
- 2,11 pH
- 3 Koulutus
- 3.1 Kalsiumnitraatti ja ammoniumvetyfosfaatti
- 3.2 Kalsiumhydroksidi ja fosforihappo
- 4 Käyttö
- 4.1 Luukudoksessa
- 4.2 Biokeraamiset sementit
- 4.3 Lääkärit
- 4.4 Muu
- 5 Viitteet
Kalsiumfosfaatin rakenne
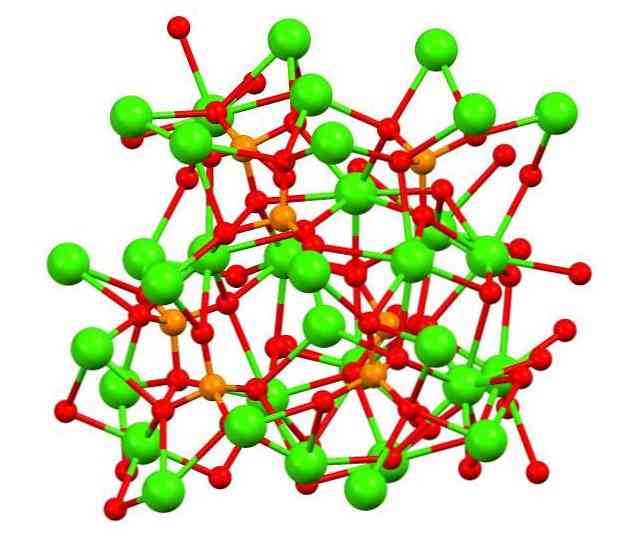
Ylemmässä kuvassa on hajakalvon fosfaatin rakenne kummallisessa valkovoidemassa, joka voi sisältää magnesiumia ja rautaa epäpuhtauksina.
Vaikka ensi silmäyksellä se saattaa tuntua monimutkaiselta, on tarpeen selventää, että malli olettaa kovalenttisen vuorovaikutuksen fosfaattien happiatomien ja kalsiummetallikeskusten välillä..
Esityksenä se on kelvollinen, mutta vuorovaikutukset ovat sähköstaattisia; eli kationit Ca2+ ovat kiinnostuneita PO-anioneista43- (Ca2+- O-PO33-). Tässä mielessä ymmärretään, miksi kuvassa kalsiumia (vihreitä palloja) ympäröivät negatiivisesti varautuneet happiatomit (punaiset pallot).
Kun ioneja on niin paljon, se ei jätä symmetristä järjestelyä tai kuviota näkyväksi. Ca3(PO4)2 Hyväksyy alhaisissa lämpötiloissa (T<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(PO4)2 (β-TCP, sen lyhenne englanniksi).
Korkeissa lämpötiloissa se puolestaan muunnetaan a-Ca-polymorfiseksi3(PO4)2 (a-TCP), jonka yksikön solu vastaa monokliinistä kiteistä järjestelmää. Jopa korkeammissa lämpötiloissa voidaan muodostaa myös polymorfinen a'-Ca3(PO4)2, joka on kuusikulmainen kiderakenne.
Amorfinen kalsiumfosfaatti
Kalsiumfosfaattia varten on mainittu kristallirakenteita, joita on odotettavissa suolalta. Se on kuitenkin kykenevä näyttämään epäsäännöllisiä ja epäsymmetrisiä rakenteita, jotka on kytketty enemmän "kalsiumfosfaattilasin" tyyppiin kuin kiteisiin sen tarkan määritelmän mukaisesti..
Kun näin tapahtuu, sanotaan, että kalsiumfosfaatilla on amorfinen rakenne (ACP, amorfinen kalsiumfosfaatti). Useat tekijät viittaavat tämän tyyppiseen rakenteeseen, joka vastaa Ca: n biologisista ominaisuuksista3(PO4)2 luun kudoksissa, sen korjaaminen ja biomimetisointi on mahdollista.
Selvittämällä sen rakenteen ydinmagneettisen resonanssin (NMR) avulla on havaittu OH-ionien läsnäolo- ja HPO42- AKT-maissa. Nämä ionit muodostuvat yhden fosfaatin hydrolyysistä:
PO43- + H2O <=> HKO42- + OH-
Tämän seurauksena AKT: n todellinen rakenne muuttuu monimutkaisemmaksi, jonka koostumusta sen ioneista edustaa kaava: Ca9(PO4)6-x(HKO4)x(OH)x. "X" ilmaisee hydraatiotason, koska jos x = 1, niin kaava olisi: Ca9(PO4)5(HKO4) (OH).
Eri rakenteet, joita PCA: lla voi olla, riippuvat Ca / P-moolisuhteista; toisin sanoen kalsiumin ja fosfaatin suhteellisista määristä, jotka muuttavat koko niiden tuloksena olevaa koostumusta.
Loput perheestä
Kalsiumfosfaatit ovat itse asiassa epäorgaanisten yhdisteiden perhe, joka puolestaan voi olla vuorovaikutuksessa orgaanisen matriisin kanssa.
Muut fosfaatit saadaan "yksinkertaisesti" muuttamalla kalsiumia mukana olevia anioneja (PO43-, HKO42-, H2PO4-, OH-) sekä kiinteän aineen epäpuhtauksien tyyppi. Näin ollen jopa yhdentoista tai useamman kalsiumfosfaatin, joista jokaisella on oma rakenne ja ominaisuudet, voi syntyä luonnollisesti tai keinotekoisesti..
Alla on joitakin fosfaatteja ja niiden rakenteita ja kemiallisia kaavoja:
-Vety- kalsiumfosfaattidihydraatti, CaHPO4∙ 2H2O: monokliininen.
-Kalsiumdivetyfosfaattimonohydraatti, Ca (H)2PO4)2∙ H2O: triklinikka.
-Vedetön dihappofosfaatti, Ca (H)2PO4)2: triklinikka.
-Ocalcium-vetyfosfaatti (OCP), Ca8H2(PO4)6: triklinikka Se on hydroksiapatiitin synteesin esiaste.
-Hydroxyapatite, Ca5(PO4)3OH: kuusikulmainen.
Fysikaaliset ja kemialliset ominaisuudet
nimet
-Kalsiumfosfaatti
-Trikalsiumfosfaatti
-Trikalsiumdifosfaatti
Molekyylipaino
310,74 g / mol.
Fyysinen kuvaus
Se on hajuton valkoinen kiinteä aine.
maku
mauton.
Sulamispiste
1670 ° K (1391 ° C).
liukoisuus
-Käytännössä liukenematon veteen.
-Liukenematon etanoliin.
-Liukenee laimeaan suolahappoon ja typpihappoon.
tiheys
3,14 g / cm3.
Taitekerroin
1629
Koulutuksen tavallinen entalpia
4126 kcal / mol.
Varastointilämpötila
2-8 ºC.
pH
6-8 vesipitoisessa suspensiossa, jossa on 50 g / l kalsiumfosfaattia.
koulutus
Kalsiumnitraatti ja vedyn ammoniumfosfaatti
Kalsiumfosfaatin valmistamiseksi tai muodostamiseksi on lukuisia menetelmiä. Yksi niistä koostuu kahden suolan, Ca (NO), seoksesta3)2∙ 4H2O ja (NH4)2HKO4, aiemmin liuotettu absoluuttiseen alkoholiin ja veteen. Yksi suola antaa kalsiumia ja toinen fosfaatti.
Tästä seoksesta ACP saostuu, joka sitten kuumennetaan uunissa 800 ° C: ssa ja 2 tunnin ajan. Tämän menetelmän tuloksena saadaan P-Ca3(PO4)2. Säätämällä huolellisesti lämpötiloja, sekoitusta ja kosketusaikoja voi tapahtua nanokristallin muodostuminen.
Polymorfin a-Ca muodostamiseksi3(PO4)2 on tarpeen lämmittää fosfaatti yli 1000 ° C: ssa. Tämä kuumennus suoritetaan muiden metalli-ionien läsnä ollessa, jotka stabiloivat tämän polymorfin riittävän hyvin sen käyttämiseksi huoneenlämpötilassa; toisin sanoen se pysyy stabiilina metatilassa.
Kalsiumhydroksidi ja fosforihappo
Kalsiumfosfaatti voidaan myös muodostaa sekoittamalla kalsiumhydroksidin ja fosforihapon liuokset happo-emäksen neutraloinnilla. Puolen päivän kypsymisen jälkeen emäliuoksissa ja niiden asianmukaista suodatusta, pesemistä, kuivaamista ja seulomista saadaan rakeinen jauhe, jossa on amorfista fosfaattia, ACP.
Tämä AKT-reaktio tuottaa korkean lämpötilan, joka muuttuu seuraavien kemiallisten yhtälöiden mukaisesti:
2ca9(HKO4) (PO4)5(OH) => 2Ca9(P2O7)0,5(PO4)5(OH) + H2O (T = 446,60 ° C)
2ca9(P2O7)0,5(PO4)5(OH) => 3Ca3(PO4)2 + 0,5H2O (T = 748,56 ° C)
Tällä tavalla saadaan P-Ca3(PO4)2, sen yleisin ja stabiili polymorfi.
sovellukset
Luukudoksessa
Ca3(PO4)2 Se on luun tuhkan tärkein epäorgaaninen aineosa. Se on osa luun korvaushoitoa, mikä selittyy sen kemiallisella samankaltaisuudella luun sisältämien mineraalien kanssa.
Kalsiumfosfaatti biomateriaaleja käytetään korjaamaan luun vikoja ja titaanimetalliproteesien pinnoitusta. Kalsiumfosfaatti kerrostuu niihin, eristetään ne ympäristöstä ja hidastetaan titaanikorroosiota.
Kalsiumfosfaatit, mukaan lukien Ca3(PO4)2, Niitä käytetään keraamisten materiaalien valmistukseen. Nämä materiaalit ovat biologisesti yhteensopivia, ja niitä käytetään tällä hetkellä palauttamaan alveolaarisen luun häviön, joka on seurausta periodontaalisesta taudista, endodontisista infektioista ja muista olosuhteista..
Niitä tulisi kuitenkin käyttää vain periaattisen luun korjaamisen nopeuttamiseen alueilla, joilla ei ole kroonista bakteeri-infektiota.
Kalsiumfosfaattia voidaan käyttää luuvirheiden korjaamiseen, kun autogeenistä luunsiirtoa ei ole mahdollista käyttää. On mahdollista käyttää sitä yksinään tai yhdessä biologisesti hajoavan ja resorboituvan polymeerin, kuten polyglykolihapon kanssa.
Biokeraamiset sementit
Kalsiumfosfaatti- sementti (CPC) on toinen biokeramiikka, jota käytetään luukudoksen korjaamiseen. Se valmistetaan sekoittamalla eri tyyppisten kalsiumfosfaattien jauhe veteen ja muodostamalla tahna. Tahna voidaan ruiskuttaa tai säätää luun vikaan tai onteloon.
Sementit valetaan, resorboidaan asteittain ja korvataan uusilla luuilla.
lääketieteellinen
-Ca3(PO4)2 Se on emäksinen suola, joten sitä käytetään antasidina neutraloimaan ylimääräistä mahahappoa ja lisäämään pH: ta. Hammastahnassa se tarjoaa kalsiumin ja fosfaatin lähteen, joka helpottaa hampaiden ja luun hemostaasin remineralisaatioprosessia.
-Sitä käytetään myös ravintolisänä, vaikka halvin tapa kalsiumin korvaamiseksi on sen karbonaatin ja sitraatin käyttö..
-Kalsiumfosfaattia voidaan käyttää tetany-, piilevän hypokalsemian ja ylläpitohoidon hoidossa. Lisäksi se on käyttökelpoinen kalsiumin lisäyksessä raskauden ja imetyksen aikana.
-Sitä käytetään radioaktiivisen isotoopin radion (Ra-226) ja strontiumin (Sr-90) saastumisen hoidossa. Kalsiumfosfaatti estää radioaktiivisten isotooppien imeytymisen ruoansulatuskanavassa, mikä rajoittaa niiden aiheuttamia vahinkoja.
toiset
-Kalsiumfosfaattia käytetään lintujen rehuna. Lisäksi sitä käytetään hammastahnoissa tartarin kontrolloimiseksi.
-Sitä käytetään paakkuuntumisenestoaineena, esimerkiksi estämään pöytäsuolan tiivistymistä.
-Se toimii jauhojen valkaisuaineena. Vaikka sianlihassa ehkäistään ei-toivottua väriä ja parannetaan paistamisen tilaa.
viittaukset
- Tung M.S. (1998) Kalsiumfosfaatit: rakenne, koostumus, liukoisuus ja stabiilisuus. Julkaisussa: Amjad Z. (eds) Kalsiumfosfaatit biologisissa ja teollisissa järjestelmissä. Springer, Boston, MA.
- Langlang Liu, Yanzeng Wu, Chao Xu, Suchun Yu, Xiaopei Wu ja Honglian Dai. (2018). "Synteesi, nano-p-trikalsiumfosfaatin karakterisointi ja hepatosellulaaristen karsinoomasolujen inhibitio", Journal of Nanomaterials, voi. 2018, artikkelin tunnus 7083416, 7 sivua, 2018.
- Combes, Kristus ja Rey, kristitty. (2010). Amorfiset kalsiumfosfaatit: synteesi, ominaisuudet ja käyttö biomateriaaleissa. Acta Biomaterialia, voi. 6 (nro 9). ss. 3362-3378. ISSN 1742-7061
- Wikipedia. (2019). Trikalsiumfosfaatti. Haettu osoitteesta: en.wikipedia.org
- Abida et ai. (2017). Trikalsiumfosfaattijauhe: Valmistus-, karakterisointi- ja tiivistysominaisuudet. Mediterranean Journal of Chemistry 2017, 6 (3), 71-76.
- Pubchem. (2019). Kalsiumfosfaatti. Haettu osoitteesta pubchem.ncbi.nlm.nih.gov
- Elsevier. (2019). Kalsiumfosfaatti. Science Direct. Haettu osoitteesta: sciencedirect.com


