Natriumkloridin (NaCl) rakenne, ominaisuudet, käyttötavat, toksisuus
natriumkloridia, kutsutaan myös tavalliseksi suolaksi tai pöytäsuolaksi, on alkalimetallinatriumin ja halogeeniklorin binaarinen epäorgaaninen suola. Se on syötävän suolan suurin komponentti ja sen mineraalimuoto tunnetaan haliteeksi. Sen molekyylikaava on NaCl ja kuvaa sen ionien stoikiometristä suhdetta (Na+ cl-) eikä erillisen molekyylin (Na-Cl)
Natriumkloridi on kiteinen valkoinen kiinteä aine, joka muodostuu natriumin, hopeanhohtaisen valkoisen metallin, joka reagoi kiivaasti veden kanssa, ja kloorielementin, myrkyllisen, syövyttävän, vaalean vihreän kaasun, kanssa..

Ylemmässä kuvassa esitetään osa NaCl-kiteistä. Miten on mahdollista, että kaksi elementtiä ovat niin vaarallisia kuin Na ja Cl2, voiko muodostaa syötävä suola? Ensinnäkin sen muodostumisen kemiallinen yhtälö on:
2Na (s) + Cl2(g) => 2NCl (s)
Vastaus on NaCl: n linkin luonteessa. Koska ne ovat ionisia, Na: n ominaisuudet+ ja Cl- ne ovat diagonaalisesti erilaisia kuin neutraalien atomiensa.
Natrium on elintärkeä elementti, mutta sen ionimuodossa. Na+ on pääasiallinen solunulkoinen kationi, jonka pitoisuus on noin 140 mEq / lt, ja yhdessä sen mukana tulevien anionien kanssa Cl- ja HCO3- (bikarbonaatti), ovat pääasiassa vastuussa osmolaarisuuden ja solunulkoisen tilavuuden arvosta.
Lisäksi Na+ on vastuussa hermoimpulssien syntymisestä ja johtamisesta hermosoluissa, sekä lihasten supistumisen aloittamisesta.
NaCl: a on käytetty muinaisista ajoista elintarvikkeiden maustamiseen ja lihan säilyttämiseen, koska se kykenee poistamaan bakteerit ja ehkäisemään pilaantumista.
Se on myös välttämätön natriumhydroksidin (NaOH) ja molekyyli- kloorin (Cl2) saattamalla NaCl reagoimaan veden kanssa hydrolyysissä:
2H2O (l) + 2 NaCl (s) => 2NaOH (ac) + Cl2(g) + H2(G)
Katodissa (-) H kerääntyy2 (g) ja NaOH. Samaan aikaan Cl kerääntyy anodiin (+)2 (G). Natriumhydroksidia käytetään saippuoiden ja kloorin valmistuksessa PVC-muovin valmistuksessa.
indeksi
- 1 Natriumkloridin rakenne
- 1.1 Yksittäinen solu
- 2 Ominaisuudet
- 2.1 Molekyylikaava
- 2.2 Molekyylipaino
- 2.3 Fyysinen kuvaus
- 2.4 Väri
- 2.5 Maku
- 2.6 Kiehumispiste
- 2.7 Sulamispiste
- 2.8 Liukoisuus veteen
- 2.9 Liukoisuus orgaanisiin liuottimiin
- 2.10 Tiheys
- 2.11 Höyrynpaine
- 2.12 Stabiilisuus
- 2.13 Hajoaminen
- 2.14 Viskositeetti
- 2.15 Korroosio
- 2,16 pH
- 3 Käyttö
- 3.1 Elintarvikkeissa
- 3.2 Teolliset käyttötavat
- 3.3 Kotona
- 3.4 Muut käyttötarkoitukset
- 3.5 Terapeuttiset käyttötarkoitukset
- 4 Myrkyllisyys
- 4.1 Nieleminen
- 4.2 Ärsytys ja fyysinen kosketus
- 5 Viitteet
Natriumkloridin rakenne
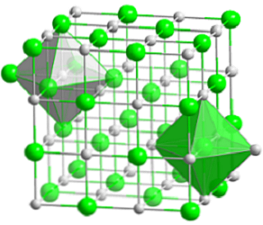
Ylemmässä kuvassa on esitetty natriumkloridin kompakti kuutiomainen rakenne. Tilavat vihreät pallot vastaavat Cl-anioneja-, valkoisina Na-kationeihin+. Huomaa, miten NaCl-kide koostuu ionien verkosta, joka on järjestetty niiden sähköstaattisilla vuorovaikutuksilla suhteessa 1: 1.
Vaikka kuvassa on palkkeja, sidokset eivät ole kovalenttisia, vaan ionisia. Palkkien käyttö on hyödyllistä, kun näytetään koordinointigeometria ionin ympärillä. Esimerkiksi NaCl: n tapauksessa kukin Na+ ympäröi kuusi Cl- (valkoinen oktaedri) ja kukin Cl- kuusi Na+ (vihreä oktaedri).
Siksi sillä on koordinaatio (6,6), jonka numerot osoittavat, kuinka monta naapuria ympäröi kutakin ionia. Oikealla oleva numero osoittaa Na: n naapureita+, kun taas vasemmalla, Cl-.
Muut esitykset jättävät pois palkkien käytön korostamaan oktaedraalisia reikiä, joita rakenteessa on, mikä johtuu kuuden Cl-anionin välisestä välitilasta.- (tai Na-kationit+) pakattu. Tämä järjestely havaitaan muissa mono- (MX) tai polyatomisissa epäorgaanisissa suoloissa, ja sitä kutsutaan gem-suolaksi..
Unitary cell
Kivisuolan yksikkösolu on kuutiometriä, mutta mitkä kuutiot edustavat sitä tarkasti yllä olevassa kuvassa? Oktaedrit antavat vastauksen. Molemmat kattavat yhteensä neljä pientä kuutiota.
Näissä kuutioissa on osia ioneista niiden pisteissä, reunoissa ja kasvoissa. Havaitaan tarkasti ioni Na+ se sijaitsee keskellä ja kaksitoista niistä reunoissa. Yhdellä reunalla oleva ioni voidaan jakaa neljän kuution kanssa. Joten on 4 Na-ionia+ (12 × 1/4 + 1 = 4).
Cl-ioneja varten-, kahdeksan sijaitsee pisteissä ja kuusi reunoissa. Koska huippuissa olevat ionit jakavat tilaa kahdeksalla muulla kuutiolla, ja reunoilla, joissa on kuusi, niissä on 4 Cl-ionia- (8 × 1/8 + 6 × 1/2 = 4).
Edellinen tulos tulkitaan seuraavasti: NaCl: n yksikkösolussa on neljä Na-kationia+ ja neljä Cl-anionia-; osuus, joka vastaa kemiallista kaavaa (Na+ kullekin Cl: lle-).
ominaisuudet
Molekyylikaava
NaCl:.
Molekyylipaino
58,44 g / mol.
Fyysinen kuvaus
Kiteinen kiinteä aine.
väri
Läpinäkyvät värittömät kiteet tai valkoinen kiteinen jauhe.
maku
suolainen.
Kiehumispiste
2,575 ºF - 760 mmHg.
1,465 ºC.
Sulamispiste
1 474 ºF (800,7 ºC).
Sekä kiehumispiste että sulamispiste heijastavat lämpöä, joka tarvitaan kiteisen retikulaarisen energian voittamiseksi. Siksi nämä mittaukset vahvistavat NaCl: n ionisen luonteen.
Liukoisuus veteen
Suurempi tai yhtä suuri kuin 100 mg / ml 68 ° F: ssa.
36,0 g / 100 ml 25 ° C: ssa.
Se on itse asiassa hygroskooppinen suola, joka säilyttää kosteuden ympäristöstä.
Liukoisuus orgaanisiin liuottimiin
0,065 g / 100 ml etanolia 25 ° C: ssa; 10 g / 100 g glyserolia 25 ° C: ssa; 2,15 g / 100 ml nestemäistä ammoniumia 40 ° C: ssa; 1,4 g / 100 ml metanolia 25 ° C: ssa; 7,15 g / 100 eteeniglykolia 25 ° C: ssa ja 5,21 g / 100 g muurahaishappoa 25 ° C: ssa.
tiheys
2,165 g / cm3 77 ° C: ssa.
Höyrynpaine
1 mmHg - 1589 ° F.
pysyvyys
Se on stabiili suositelluissa säilytysolosuhteissa.
hajoaminen
Korkeisiin lämpötiloihin kuumennettaessa se hajoaa suolahapon ja dinatriumoksidin höyryjä.
viskositeetti
Tyydyttyneiden liuosten viskositeetti 1,93 mPa-s.
korroosio
Se on syövyttävää monille metalleille.
pH
6,7 - 7,3 vesiliuoksessa.
sovellukset
Elintarvikkeissa
-Natriumkloridia on käytetty muinaisista ajoista elintarvikkeiden makuun ja sen säilyttämiseen. Lihan suolaus on tapa säilyttää se bakteeritoiminnalta, koska se viivästyttää proteiinin hajoamista.
-Toisaalta suola lisää osmolaarisuutta lihan ympärillä, mikä aiheuttaa imeytymisen osmoosin avulla niiden bakteerien veteen, jotka aiheuttavat sen eliminaation.
Teolliset käyttötarkoitukset
Elintarviketeollisuus
-Elintarviketeollisuudessa suolaa käytetään makuainetta tehostavana aineena, fermentointia säätelevänä lisäaineena, tekstuurin säätöaineena ja värinkehittäjänä. Suolaa lisätään esimerkiksi pekonin, kinkun ja muiden lihavalmisteiden värin korostamiseksi.
-Suola toimii sideaineena makkaroiden valmistuksessa. Se edistää lihan, rasvan ja kosteuden muodostaman sideaineen muodostumista.
-Jauhojen valmistuksessa leivän valmistuksessa lisätään suolaa keittämisen aikana leivän taikinan käymisen nopeuden säätämiseksi. Sitä käytetään myös gluteenin vahvistamiseen ja arominvahventeena sekä leivottujen tavaroiden täyttämiseen.
-Sitä käytetään aamiaismurojen, sekoitettujen tai valmistettujen jauheiden, ranskanperunoiden, koirien ja kissojen aterioiden valmistuksessa jne..
Kemiallisten tuotteiden synteesi
-Natriumkloridia käytetään raaka-aineena natriumhydroksidin ja kloorin valmistuksessa, joka puolestaan on hyödyllinen monissa kemianteollisuudessa.
-Suolaa käytetään erilaisten metallien, esimerkiksi alumiinin, kuparin, teräksen ja vanadiinin, jalostuksessa. Sitä käytetään myös natriumkloraatin valmistamiseen, jota käytetään myöhemmin klooridioksidin synteesissä, happipohjaisena valkaisuaineena. Klooridioksidi on vähemmän haitallista ympäristölle kuin muut valkaisuaineet.
Nahateollisuudessa
-Suolaa käytetään estämään bakteerien vaikutus ihon sisällä sekä auttamaan sen rehydraatiossa.
Tekstiiliteollisuudessa
-Suolaa käytetään kankaiden värjäyksessä. Sitä käytetään suolaliuoksena orgaanisten epäpuhtauksien poistamiseksi ja positiivisen varauksen aikaansaamiseksi kankaiden pinnalle, joka mahdollistaa negatiivisesti varautuneiden väriaineiden liitoksen.
Öljyteollisuudessa
-Öljyn ja kaasun etsinnässä suola on tärkeä osa porausnesteitä. Sitä käytetään porausnesteiden flokkuloitumiseen ja tiheyden lisäämiseen, mikä mahdollistaa ylittävän kaasun korkean paineen ylittävissä kuoppissa. Lisäksi suola ylläpitää porausnesteen kylläisyyttä.
-Suola auttaa tiivistämään maaperää, johon tiet on rakennettu. Vähentää maaperän aiheuttamaa siirtymää kosteuden ja autoliikenteen muutoksilla.
Kotona
Suolaa on käytetty hankaamalla pintojen, kattiloiden ja pannujen puhdistuksessa. Myös muotin ehkäisyyn ja tahranpoistoon. Sitä käytetään myös monissa shampoo- ja hammastahnaajissa.
Muut käyttötarkoitukset
Teillä
-Lumisateiden varrella ennakoidaan suolavedellä, mikä estää jään liittymisen tien pintaan. Sulatukseen käytetään suolaliuoksen ja suolan seosta, ja toisinaan lisätään muita kemiallisia komponentteja, kuten magnesiumia tai kalsiumkloridia. Suolan ja suolaliuoksen käyttö ei ole tehokasta alle -10 ºC: n lämpötiloissa.
Kun lisätään suolaa, kryoskooppipisteessä, liuosten kollektiivisessa ominaisuudessa, on vähentynyt, mikä estää jonkinlaista jään muodostumista.
-Hygroskooppisen tilansa vuoksi suolaa käytetään halpana kuivausaineena.
Veden pehmenemisessä käytetyissä hartseissa
Kovassa vedessä on kalsiumia ja magnesiumia, jotka estävät saippuan vaikutuksen ja tuottavat emäksisten materiaalien kerrostumia eri laitteissa ja putkissa. Veden pehmenemisessä käytetään ioninvaihtohartseja. Suolaa käytetään hartsien valmistuksessa ja regeneroinnissa.
Palosammuttimissa
Palonsammuttimissa käytetään natriumkloridia tulipalojen torjumiseksi, joissa on palavia metalleja, kuten magnesiumia, kaliumia, natriumia ja NK-seoksia.
Suola toimii jäähdytyselementtinä ja myös murskaimena, joka rajoittaa hapen pääsyä tuleen.
Lasit
Natriumkloridin kiteitä käytetään optisissa komponenteissa, kuten ikkunoissa ja prismoissa, erityisesti infrapunavalossa. Koska suola on kuitenkin hyvin hygroskooppinen, esiintyy eräänlainen pakkas, joka peittää linssit. Tästä syystä natriumkloridilinssit on korvattu sinkkisenidin (ZnSe) linsseillä..
Terapeuttiset käyttötarkoitukset
Täydentää suolojen puuttumista kehossa
-Kun on Na: n kehon heikkeneminen+, on korvattava ekstrasellulaarisen osmolariteetin, hermon johtumisen ja lihaskontraktioiden ylläpitämiseksi.
-NaCl: a käytetään natriumin ja kloorin puutteen hoitoon ja ehkäisyyn, joka johtuu liiallisesta hikoilusta altistettaessa korkeille lämpötiloille. Sitä käytetään myös liialliseen diureesiin tai liialliseen suolanottoon.
-045% NaCl-liuoksen parenteraalista antamista käytetään hyperosmolaarisen diabeteksen hoidossa. Se täyttää rehydratointitoiminnon ja auttaa arvioimaan munuaisfunktion tilaa.
-Hypertonisten liuosten injektiot, joiden NaCl-pitoisuus on suurempi kuin 0,9 paino-%,
-Niitä käytetään silloin, kun Na on heikentynyt voimakkaasti+, on olennaisen ionin palauttaminen. Tämä hyponatremia voi olla seurausta vapaan elektrolyytin käsittelystä tai Na-pitoisuudesta+.
Hyponatremiaa voi aiheuttaa myös liiallinen vedenotto, jota ei valvota riittämätön munuaisten toiminta.
Hoidoissa ja epätavallisissa käyttötavoissa
-NaCl-inhalaatioliuoksia käytetään sumuttamisen aikana käytettyjen lääkkeiden laimentamiseksi. Sitä käytetään myös henkitorven pesuun ja kasteluun. 0,9% suolaliuosta, jota käytetään nenäsuihkeissa.
-20% NaCl-liuoksia käytetään sisäisen munasarjojen transabdominaalisessa asennuksessa, mikä aiheuttaa myöhäisen abortin raskauden toisen kolmanneksen aikana.
-Natriumkloridia voidaan käyttää paikallisena antiseptisenä aineena. Osmoottisen kapasiteetinsa ansiosta se pystyy dehydratoimaan suuren määrän viruksia ja bakteereita palamattomassa tilassa; Siksi sitä käytetään kivuliaana antiseptisenä haavojen desinfioimiseksi.
myrkyllisyys
nieleminen
Sillä on vain haitallinen vaikutus terveyteen, jos saanti on korkea ja pitkään. Näissä olosuhteissa hypernatremiaa esiintyy, mikä johtaisi ekstrasellulaarisen tilavuuden kasvuun, mikä johtaisi korkeaan verenpaineeseen.
Ärsytys ja fyysinen kosketus
Sillä on myrkyllinen vaikutus vain, jos inhalaatio on erittäin korkea. Ihokosketuksessa liiallinen muoto voi aiheuttaa sen kuivuuden. Lopuksi se aiheuttaa hetkellisen ärsytyksen joutuessaan kosketuksiin silmien kanssa.
viittaukset
- Shiver & Atkins. (2008). Epäorgaaninen kemia (Neljäs painos, sivut 84, 90, 93, 263). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. Kemia. (8. painos). CENGAGE Learning, s. 482-483.
- Natriumkloridi (2018). Natriumkloridi: hyödyt, käyttötarkoitukset, ominaisuudet, riskit. Otettu: clorurodesodio.org
- Pubchem. (2018). Natriumkloridi. Haettu osoitteesta pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Natriumkloridi. Otettu: en.wikipedia.org
- American Elements. (2018). Natriumkloridi. Otettu: americanelements.com


