Peltikloridi (SnCl2) Ominaisuudet, rakenne, käyttö ja riskit
tinakloridi (II) tai tinakloridi, kemiallinen kaava SnCl2, on valkoinen kiteinen kiinteä yhdiste, tinan ja väkevän suolahapon liuoksen tuote: Sn (s) + 2HCI (conc) => SnCl2(aq) + H2(G). Sen synteesimenetelmä (valmistus) koostuu tina-arkkien osien lisäämisestä hapon kanssa reagoimiseksi.
Tinaosien lisäämisen jälkeen se suorittaa dehydratoinnin ja kiteytyksen, kunnes saadaan epäorgaaninen suola. Tässä yhdisteessä tina on menettänyt kaksi elektronia valenssikuoristaan muodostaakseen sidoksia klooriatomeihin.
Tämä voidaan ymmärtää paremmin, jos tarkastellaan tinan valenssikokoonpanoa (5s25px2pja0pz0), joista elektronien pari, joka on kiertoradalla px annetaan protoneille H+, jotta muodostettaisiin vedyn diatomi-molekyyli. Eli tämä on redox-tyyppinen reaktio.
indeksi
- 1 Fysikaaliset ja kemialliset ominaisuudet
- 1.1 Valencian kokoonpano
- 1.2 Reaktiivisuus
- 1.3 Pelkistävä toiminta
- 2 Kemiallinen rakenne
- 3 Käyttö
- 4 Riskit
- 5 Viitteet
Fysikaaliset ja kemialliset ominaisuudet
SnCl-linkit2 Ovatko ne ionisia tai kovalenttisia? Tina (II) kloridin fysikaaliset ominaisuudet estävät ensimmäisen vaihtoehdon. Tämän yhdisteen sulamis- ja kiehumispisteet ovat 247 ° C ja 623 ° C, mikä osoittaa heikot molekyylien väliset vuorovaikutukset, yleinen tosiasia kovalenttisille yhdisteille..
Sen kiteet ovat valkoisia, mikä tarkoittaa nollaa absorptiota näkyvässä spektrissä.
Valencian kokoonpano
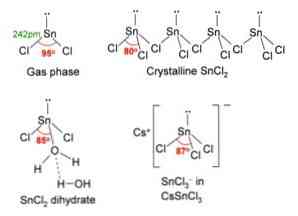
Yllä olevassa kuvassa on esitetty vasemmassa yläkulmassa eristetty SnCl-molekyyli2.
Molekyyligeometrian tulisi olla tasainen, koska keskiatomin hybridisaatio on sp2 (3 orbital sp2 ja puhdas p-orbitaali kovalenttisten sidosten muodostamiseksi), mutta vapaa elektronien pari vie tilavuuden ja työntää klooriatomit alas, jolloin molekyyli on kulma-geometria.
Kaasufaasissa tämä yhdiste eristetään, joten se ei ole vuorovaikutuksessa muiden molekyylien kanssa.
Elektroniikkaparin menetys orbitaalisessa px, tina muunnetaan ioniksi Sn2+ ja sen tuloksena oleva elektroninen kokoonpano on 5s25px0pja0pz0, kaikki sen p orbitaalit ovat käytettävissä hyväksymään linkkejä muista lajeista.
Cl-ionit- koordinoi Sn-ionin kanssa2+ tinakloridin aikaansaamiseksi. Tämän suolan tina-elektroninen kokoonpano on 5 s25px2pja2pz0, pystyy hyväksymään toisen elektroniparin sen vapaassa orbitaalisessa pz.
Voit esimerkiksi hyväksyä toisen Cl-ionin-, muodostetaan trigonaalisen tason geometriakompleksi (pyramidi, jossa on kolmiomainen pohja) ja negatiivisesti varautunut [SnCl3]-.
reaktiivisuus
SnCl2 jolla on korkea reaktiivisuus ja taipumus käyttäytyä Lewis-hapon (elektronireseptorin) tavoin valenssilähteensä suorittamiseksi.
Aivan kuten se hyväksyy Cl-ionin-, sama tapahtuu veden kanssa, joka "hydratoi" tinaatomia kytkemällä vesimolekyylin suoraan tinaan, ja toinen vesimolekyyli muodostaa vetyliitoksen vuorovaikutuksia ensimmäisen.
Tämän seurauksena SnCl2 se ei ole puhdas, vaan se on koordinoitu veden kanssa sen dihydratoidussa suolassa: SnCl2· 2H2O.
SnCl2 Se on hyvin liukoinen veteen ja polaarisiin liuottimiin, koska se on polaarinen yhdiste. Sen liukoisuus veteen, pienempi kuin sen massa, aktivoi kuitenkin hydrolyysireaktion (vesimolekyylin repeämä), jolloin muodostuu emäksinen ja liukenematon suola:
SnCl2(aq) + H2O (l) <=> Sn (OH) Cl (s) + HCI (aq)
Kaksoissuoli osoittaa, että tasapaino on muodostunut, suosittu vasemmalle (kohti reagensseja), jos HCI-pitoisuudet kasvavat. Tätä varten SnCl-ratkaisut2 käytettynä on happo-pH, jotta vältetään hydrolyysin ei-toivotun suolatuotteen saostuminen.
Pelkistävä toiminta
Reagoi ilman hapen kanssa muodostaen tina (IV) kloridia tai tina-kloridia:
6 SnCl2(aq) + O2(g) + 2H2O (l) => 2SnCl4(aq) + 4Sn (OH) Cl (s)
Tässä reaktiossa tina hapettaa muodostaen sidoksen elektronegatiiviseen happiatomiin ja lisää sen sidosten määrää klooriatomien kanssa.
Yleensä halogeenien (F, Cl, Br ja I) elektronegatiiviset atomit stabiloivat Sn (IV) -yhdisteiden sidokset ja tämä seikka selittää, miksi SnCl2 se on pelkistävä aine.
Kun se hapettaa ja menettää kaikki valenssielektronit, Sn-ioni4+ se pysyy 5s: n kokoonpanossa05px0pja0pz0, on elektronien pari kiertoradalla 5, joita on vaikeimmin "kaapattu".
Kemiallinen rakenne
SnCl2 esittelee ortorombista tyyppiä olevaa kristallirakennetta, joka on samanlainen kuin sahojen rivit, joissa hampaiden kärjet ovat klorideja.
Jokainen rivi on SnCl-ketju3 Cl-sillan muodostaminen toisen Sn-atomin kanssa (Cl-Sn (Cl)2-Cl- ···, kuten yllä olevassa kuvassa näkyy. Kaksi ketjua, jotka ovat yhteydessä Sn-Cl-tyypin heikkoihin vuorovaikutuksiin, muodostavat yhden kerroksen järjestelystä, joka on päällekkäin toisella kerroksella ja niin edelleen, kunnes kiteinen kiinteä aine on määritelty.
Vapaa elektronipari 5s2 aiheuttaa vääristymiä rakenteessa, koska se vie määrän (sähköisen pilven määrä).
Sn: llä voi olla yhdeksän koordinaatioluku, joka on sama kuin yhdeksän naapurin kanssa, piirustamalla trigonaalista prismaa, joka sijaitsee geometrisen kuvan keskellä ja Cl pisteissä, muiden Cl: n lisäksi kussakin prisman neliön kasvot.
Tämä on helpompi havaita, jos harkitaan ketjua, jossa Sn (tummanharmaat pallot) osoittavat ylöspäin, ja siihen liittyvät kolme Cl: tä muodostavat kolmiomaisen lattian, kun taas kolme ylempää Cl: tä muodostavat kolmion katon.
sovellukset
Orgaanisessa synteesissä sitä käytetään pelkistävänä aineena aromaattisille nitroyhdisteille (Ar-NO2 à Ar-NH2). Koska sen kemiallinen rakenne on laminaarinen, se käyttää maailmassa orgaanisten reaktioiden katalyysia, minkä lisäksi se on potentiaalinen katalyyttisen tuen ehdokas..
Sen pelkistävää ominaisuutta käytetään kultayhdisteiden läsnäolon määrittämiseen, lasien päällystämiseen hopeapeileillä ja antioksidanttina.
Myös sen molekyylimuodossaan trigonaalinen pyramidi (: SnX3- M+) käytetään Lewis-emäksenä suuren määrän yhdisteiden (kuten Pt-klusterikompleksin) synteesille3sn8cl20, jossa elektroniton pari koordinoidaan Lewisin hapon kanssa).
riskejä
SnCl2 Se voi vahingoittaa valkosoluja. Se on syövyttävää, ärsyttävää, syöpää aiheuttavaa, ja sillä on suuri kielteinen vaikutus meriekosysteemejä eläviin lajeihin.
Se voi hajota korkeissa lämpötiloissa ja vapauttaa haitallisen kloorikaasun. Kosketuksessa erittäin hapettavien aineiden kanssa se laukaisee räjähdysvaarallisia reaktioita.
viittaukset
- Shiver & Atkins. (2008). Epäorgaaninen kemia sisään Ryhmän 14 elementit (neljäs painos., sivu 329). Mc Graw Hill.
- ChemicalBook. (2017). Haettu 21. maaliskuuta 2018 ChemicalBookista: chemicalbook.com
- Pubchem. (2018). Tiinikloridi. Haettu 21. maaliskuuta 2018 osoitteesta PubChem: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2017). Tina (II) kloridi. Haettu 21. maaliskuuta 2018 Wikipediasta: en.wikipedia.org
- E. G. Rochow, E. W. (1975). Germaniumin kemia: Tina ja lyijy (ensimmäinen toim.). p-82,83. Pergamom Press.
- F. Hulliger. (1976). Kerrostyyppisten vaiheiden rakennekemia. P-120121. D. Reidel Publishing Company.



