Alumiinikloridin (AlCl3) kemiallinen rakenne, ominaisuudet, käyttö
alumiinikloridi tai alumiinitrikloridi (AlCl3) on binäärinen suola, joka muodostuu alumiinista ja kloorista. Joskus se näkyy keltaisena jauheena, koska se aiheuttaa epäpuhtauksia rauta (III) kloridin läsnäolon vuoksi.
Se saadaan yhdistämällä sen elementit. Alumiini, jolla on kolme elektronia viimeisellä energian tasollaan (perhe IIIA), pyrkii tuottamaan ne metallisen luonteensa vuoksi. Kloori, jossa on seitsemän elektronia viimeisellä energian tasollaan (VIIA-perhe), pyrkii saamaan ne täydentämään oktettia.
On katsottu, että alumiinin ja kloorin välisen sidoksen muodostuminen alumiinitrikloridissa on kovalenttinen, vaikka se on metallin ja ei-metallin välinen liitos..
Alumiinikloridia on kahdenlaisia:
- Vedetön alumiinikloridi. AICI3.
- Alumiinikloridiheksahydraatti. AICI3. 6H2O. Tämä yhdiste löytyy kiinteästä tai liuosmuodosta.
indeksi
- 1 Kemiallinen rakenne
- 2 Ominaisuudet
- 2.1 Fyysinen
- 2.2 Kemiallinen
- 3 Käyttö
- 4 Riskit: mahdolliset vaikutukset
- 5 suositusta
- 6 Viitteet
Kemiallinen rakenne
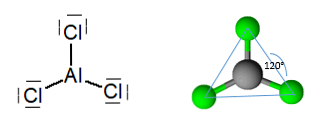
Vedetön alumiinitrikloridi on molekyyli, jossa on tasomainen trigonaalinen geometria ja jonka kulma on 120 °, joka vastaa atomihybridisointisuihkua2.
Molekyyli on kuitenkin järjestetty muodossa dimeerejä, jossa klooriatomi lahjoittaa pari elektronia sidosten muodostamiseksi. Näitä kutsutaan koordinoiduiksi kovalenttisiksi sidoksiksi.
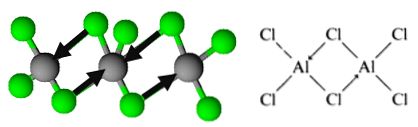
Näin päätellään alumiinitriklorididimeerien organisaatiosta.
Tämä organisaatio sallii yhdisteen muodostaa dimeeristen kerrosten verkkoja. Kun vettä kaadetaan kiinteään alumiinitrikloridiin, ne eivät hajoa odotetulla tavalla ionisista yhdisteistä, vaan ne menevät voimakkaasti hydrolyysiin.
Päinvastoin laimennetussa vesiliuoksessa ovat koordinoituneet ionit [Al (H2O)6]+3 ja kloridi. Nämä rakenteet ovat hyvin samankaltaisia kuin diboraanin rakenteet.
Tällä tavoin sinulla on kaava Al2cl6
Jos mitataan tämän yhdisteen muodostavien atomien elektronegativiteetin ero, voidaan havaita seuraavat:
Alumiini-Al: lle elektronegatiivisuuden arvo on 1,61 C ja kloorin arvo on 3,16 C. Elektronegativiteetin ero on 1,55 C.
Sitoutumisteorian sääntöjen mukaan yhdisteelle, joka on ioninen, täytyy olla ero niiden atomien elektronegativiteetissa, jotka muodostavat sidoksen arvoksi, joka on suurempi tai yhtä suuri kuin 1,7 C.
Al-Cl-sidoksen tapauksessa elektronegativiteetin ero on 1,55 C, mikä antaa alumiinitrikloridille kovalenttisen sidosjärjestelyn. Tämä pieni arvo voidaan liittää molekyylin esittämiin koordinoituihin kovalenttisiin sidoksiin.
ominaisuudet
fyysinen
ulkomuoto: valkoinen kiinteä aine, joskus keltainen, johtuen ferrikloridin aiheuttamista epäpuhtauksista
tiheys: 2,48 g / ml
Molaarinen massa133,34 g / mol
sublimaatio: sublimoituu 178 ° C: ssa, joten sen sulamis- ja kiehumispisteet ovat hyvin alhaiset.
ajo: johtaa huonosti sähköä.
liukoisuus: se ei liukene veteen, koska se on Lewisin happo. Se liukenee orgaanisiin liuottimiin, kuten bentseeniin, hiilitetrakloridiin ja kloroformiin.
kemiallinen
Vedessä alumiinitrikloridi hydrolysoidaan, jolloin muodostuu HCl ja hydroniumioni ja alumiinihydroksidi:
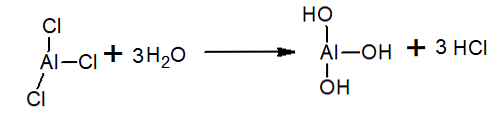
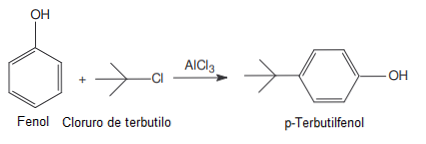
Sitä käytetään Friedel-Crafts-reaktioissa katalysaattorina (aine, joka voidaan ottaa talteen reaktion lopussa, koska se vain nopeuttaa, hidastaa tai aloittaa reaktion).
Se on syövyttävä aine.
Hajoamisen yhteydessä, kun se reagoi voimakkaasti veden kanssa, se tuottaa alumiinioksidia ja vaarallisia kaasuja, kuten kloorivetyä.
sovellukset
- antiperspirantti.
- Katalyytti Friedel-Craftsin asyloinnissa ja alkyloinnissa.
Riskit: mahdolliset vaikutukset
- Se on syövyttävä aine, aiheuttaa ihon palovammoja ja vakavia silmävaurioita.
- Reagoi kiivaasti veden kanssa.
- Se on ympäristölle vaarallista.
- Erittäin myrkyllistä vesieliöille.
suosituksia
Vältä altistumista tuotteelle ilman tarvittavia turvatoimenpiteitä. On käytettävä suojalaseja, käsineitä, asianmukaista vaatetusta, peitekenkää.
Jos hengität. Pölyn hengittäminen voi ärsyttää hengitysteitä aineen syövyttävän luonteen vuoksi. Oireita ovat kurkkukipu, yskä ja hengenahdistus. Keuhkopöhön oireet voivat olla myöhäisiä ja vakavat tapaukset voivat olla kuolemaan johtavia. Siirrä uhri ilmavaan paikkaan ilman epäpuhtauksia. antaa tarvittaessa keinotekoista hengitystä. Jos sinulla on hengitysvaikeuksia, anna happea. Soita lääkärille.
Ihokosketuksessa. AlCl3 Se on syövyttävää. Se voi aiheuttaa ärsytystä tai palovammoja punoituksella ja kivulla. Pese välittömästi kosketuksiin runsaalla vedellä vähintään 20 minuutin ajan. Älä neutraloi tai lisää muita aineita kuin vettä. Poista saastunut vaatetus ja pese se ennen uudelleenkäyttöä. Ota välittömästi yhteys lääkäriin loukkaantumisen yhteydessä.
Roiskeet silmiin. AlCl3 Se on syövyttävää. Se aiheuttaa voimakasta kipua, näön hämärtymistä ja kudosvaurioita. Huuhtele silmät välittömästi vedellä vähintään 20 minuutin ajan ja pidä silmäluomet auki, jotta silmäluomen koko silmä ja kudokset poistuvat. Silmien huuhtelu muutamassa sekunnissa on välttämätöntä, jotta saavutetaan mahdollisimman tehokas. Jos sinulla on piilolinssejä, poista ne ensimmäisten 5 minuutin kuluttua ja jatka silmien huuhtelua. Ota yhteys lääkäriin. Se voi aiheuttaa vakavia vaurioita sarveiskalvolle, sidekalvolle tai muille silmän osille.
Nieleminen. AlCl3 Se on syövyttävää. Palaminen voi aiheuttaa kipua suussa ja ruokatorvessa ja limakalvojen palovammoja. Se voi aiheuttaa ruoansulatuskanavan epämukavuutta vatsakipu, pahoinvointi, oksentelu ja ripuli. ÄLÄ KÄYTÄ VOMITOINTIA. Huuhtele suu ja anna vettä juoda. Älä koskaan anna mitään suun kautta tajuttomalle henkilölle. Soita lääkärille. Jos oksentelu tapahtuu spontaanisti, aseta uhri puolelleen, jotta imeytymisriski vähenee.
Ihmiset, joilla on nykyisiä ihosairauksia tai silmäongelmia tai hengitysvaikeuksia, voivat olla alttiimpia aineen vaikutuksille
AlCl-yhdisteen pakkaus ja varastointi3 on tehtävä tuuletetuissa, puhtaissa ja kuivissa paikoissa.
viittaukset
- Kemiallinen kirja, (2017), alumiinikloridi. Palautettu osoitteesta chemicalbook.com
- cosmos verkossa, cosmos.com.mx
- Sharpe, A.G., (1993), Organic Chemistry, Espanja, Toimituksellinen Reverté, S.A..
- F., (2017), AlCl-alumiinikloridi3, Insignia. Otettublog.elinsignia.com.
- TriHealth, (2018), alumiinitrikloridi, viimeisin päivitys, 4. maaliskuuta 2018, haettu osoitteesta trihealth.adam.com.
- RxWiki, (s.f), alumiinikloridi, haettu osoitteesta rxwiki.com.


