Vety- sulfidin (H2S) ominaisuudet, riskit ja käyttötavat
vetysulfidi on yleinen nimi, jossa on rikkivetyä (H2S). Sitä voidaan pitää hydratsidihappona liuoksessa (H2S (aq).
Sulfhydryylihapon huomioiminen annetaan huolimatta tämän kemiallisen yhdisteen vähäisestä liukoisuudesta veteen. Sen rakenne on esitetty kuvassa 1 (EMBL-EBI, 2005).
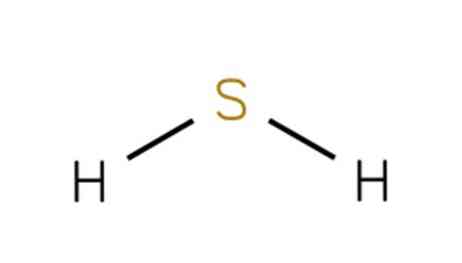
Siksi vetysulfidi on liukeneva lievästi veteen. Kun se on liuennut, se muodostaa happosulfidionin tai hydrosulfidin (HS-). Vety- sulfidin tai vetysulfidin vesiliuos on väritön ja ilmassa altistettuna hitaasti hapettaa alkuainerikkiä, joka ei liukene veteen.
Rikki dianioni S2- se on olemassa vain voimakkaasti emäksisissä vesiliuoksissa; Se on poikkeuksellisen yksinkertainen, kun pKa> 14.
H2S syntyy käytännössä silloin, kun alkuaine rikki joutuu kosketukseen orgaanisen materiaalin kanssa, erityisesti korkeissa lämpötiloissa. Vety- sulfidi on kovalenttinen hydridi, joka liittyy kemiallisesti veteen (H2O), koska happi ja rikki tuotetaan samassa ryhmässä kuin jaksollinen taulukko.
Se johtaa usein siihen, että bakteerit hajottavat orgaanisen aineen hapen puuttuessa, kuten suot ja viemärit (yhdessä anaerobisen pilkkomisprosessin kanssa). Sitä esiintyy myös tulivuoren kaasuissa, maakaasussa ja joissakin kaivojen vesissä.
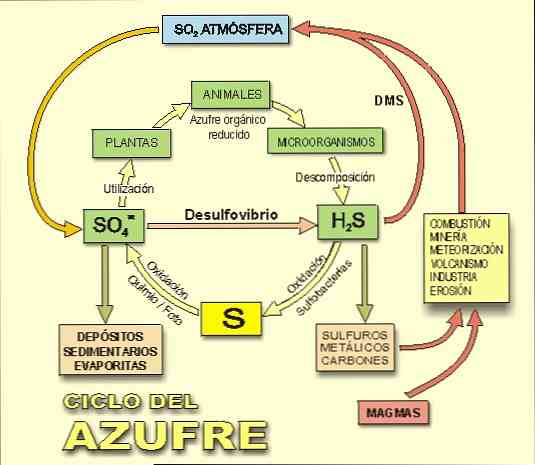
On myös tärkeää muistaa, että rikkivety on keskeinen osa rikkisykliä, rikin biogeokemiallista kierrosta maapallolla (kuva 2)..
Kuten edellä mainittiin, rikkipäästöjä vähentävät ja sulfaatin pelkistävät bakteerit tuottavat hapetusenergiaa vedystä tai orgaanisista molekyyleistä hapen poissa ollessa pelkistämällä rikkiä tai sulfaatti vetysulfidiksi.
Muut bakteerit vapauttavat rikkivetyä rikkipitoisia aminohappoja. Useat bakteeriryhmät voivat käyttää vety- sulfidia polttoaineena, hapettamalla se alkuaineeksi tai sulfaatiksi hapen tai nitraatin avulla hapettimena.
Puhdas rikki-bakteerit ja vihreät rikki-bakteerit käyttävät fotosynteesissä vetysulfidia elektronidonorina, jolloin syntyy alkuainerikkiä.
Itse asiassa tämä fotosynteesimuoto on vanhempi kuin sinilevien, levien ja kasvien tila, joka käyttää vettä elektronidonorina ja vapauttaa happea (Human Metabolome Database, 2017).
indeksi
- 1 Kun tuotetaan vetyä?
- 2 Fysikaaliset ja kemialliset ominaisuudet
- 3 Reaktiivisuus ja vaarat
- 3.1 Hengitys
- 3.2 Ihokosketus
- 3.3 Silmäkosketus
- 4 Käyttö
- 4.1 1 - Rikin valmistus
- 4.2 2- Analyyttinen kemia
- 4.3 3 - Muut käyttötarkoitukset
Kun tuotetaan vety- sulfidia?
Vety- sulfidi (H2S) esiintyy luonnollisesti raakaöljyssä, maakaasussa, tulivuorissa ja kuumissa lähteissä. Se voi myös johtua orgaanisen aineen bakteriaalisesta hajoamisesta. Sitä tuottaa myös ihmis- ja eläinjätteet.
Suussa ja ruoansulatuskanavassa esiintyvät bakteerit tuottavat rikkivetyä bakteereista, jotka hajottavat kasvi- tai eläinproteiineja sisältäviä aineita.
Vety- sulfidi voi johtua myös teollisuustoiminnasta, kuten elintarvikkeiden jalostuksesta, koksiuunista, kraft-paperitehtaista, parkituslaitoksista ja öljynjalostamoista (myrkyllisten aineiden ja tautien rekisterin virasto, 2011)..
Fysikaaliset ja kemialliset ominaisuudet
Vety- sulfidi on väritön kaasu, jolla on vahva hajunmunien haju. Vety- sulfidin vesiliuos on väritön ilman ominaista aromia.
Yhdisteen molekyylipaino on 34,1 g / mol, vesiliuoksen tiheys on 1,343 g / ml. Sen sulamispiste on -82 ° C ja kiehumispiste -60 ° C. Se liukenee lievästi veteen, sillä se voi liuottaa vain 4 grammaa litraa kohti tätä liuotinta 20 ° C: ssa (Royal Society of Chemistry, 2015).
Vety- sulfidi reagoi happona ja pelkistävänä aineena. Se räjähtää kosketuksessa hapen difluoridin, bromipentafluoridin, klooritrifluoridin, diklooridioksidin ja hopeafulminaatin kanssa. Se voi syttyä ja räjähtää, kun se altistuu kuparijauheelle hapen läsnä ollessa.
Se voi reagoida samalla tavalla muiden jauhemaisten metallien kanssa. Se sytytetään kosketuksessa metallioksidien ja peroksidien kanssa (bariumperoksidi, kromitrioksidi, kuparioksidi, lyijydioksidi, mangaanidioksidi, nikkelioksidi, hopeaoksidi, hopeaoksidi, talliumtrioksidi, natriumperoksidi, elohopeaoksidi, kalsiumoksidi) \ t.
Se sytytetään hopeabromaatilla, lyijy (II) hypokloriitilla, kuparikromaatilla, typpihapolla, lyijyoksidilla (IV) ja oksidilla. Se voi syttyä, jos se kulkee ruosteisten rautaputkien läpi. Reagoi eksotermisesti emästen kanssa.
Kalkkikalkin, natriumhydroksidin, kaliumhydroksidin, bariumhydroksidin reaktion lämpö voi aiheuttaa reagoimattoman osan syttymisen tai räjähdyksen ilman / hapen läsnä ollessa (HYDROGEN SULFIDE, 2016).
Reaktiivisuus ja vaarat
H2S pidetään stabiilina yhdisteenä, vaikka se on erittäin helposti syttyvä ja erittäin myrkyllinen.
Yhdiste on ilmaa raskaampaa ja voi kuljettaa huomattavan etäisyyden sytytyslähteeseen ja varmuuskopioida. Voi muodostaa räjähtäviä seoksia ilman kanssa laajalla alueella.
Se reagoi räjähdysmäisesti bromipentafluoridin, klooritrifluoridin, typen trijodidin, typpitrikloridin, happidifluoridin ja fenyylidiatsoniumkloridin kanssa.
Kuumentuessaan hajoamiseen se säteilee erittäin myrkyllisiä rikkioksidihöyryjä. Yhteensopimaton monien materiaalien kanssa, mukaan lukien voimakkaat hapettimet, metallit, voimakas typpihappo, bromipentafluoridi, klooritrifluori, typen trijodidi, typpitrikloridi, happidifluoridi ja fenyylidiatsoniumkloridi.
Vety- sulfidi (H2S) on vastuussa monista työperäisen myrkyllisen altistumisen tapauksista, erityisesti öljyteollisuudessa. H: n kliiniset vaikutukset2S riippuu sen pitoisuudesta ja altistuksen kestosta.
H2S on välittömästi kuolemaan, kun pitoisuudet ovat yli 500–1000 osaa miljoonaa (ppm), mutta altistuminen pienemmille pitoisuuksille, kuten 10–500 ppm, voi aiheuttaa erilaisia hengityselinten oireita, jotka vaihtelevat nuhasta akuuttiin hengitysvajeeseen.
H2S voi myös vaikuttaa moniin elimiin, mikä aiheuttaa tilapäisiä tai pysyviä häiriöitä hermo-, sydän-, munuais-, maksan ja hematologisissa järjestelmissä.
Esitetään työssä altistuminen H: lle2S, joka johtaa useiden elinten osallistumiseen, akuuttiin hengityselinten vajaatoimintaan, keuhkokuumeiden ja akuutin sepsiksen kaltaiseen shokiin. Tässä tapauksessa potilaalle kehittyi myös lievä obstruktiivinen ja rajoittava keuhkosairaus ja perifeerinen neuropatia (Al-Tawfiq, 2010).
hengitysteitse
Jos hengität, ota se ulkona ja pidä se levossa miellyttävässä asennossa hengittääksesi. Jos ei hengitä, anna keinotekoinen hengitys. Jos hengitys on vaikeaa, koulutetun henkilöstön tulee antaa happea.
Ihokosketus
Jos iho joutuu iholle, se on pestävä runsaalla vedellä. Paineistettu neste voi aiheuttaa jäätymisen. Jos altistuminen on paineistetulle nesteelle, pakastusvyöhyke on lämmitettävä välittömästi lämpimällä vedellä, joka on enintään 41 ° C.
Veden lämpötilan on oltava normaalille iholle siedettävä. Ihon lämpeneminen tulee säilyttää vähintään 15 minuutin ajan tai kunnes normaali väritys ja tunne palaa kärsivälle alueelle. Jos kyseessä on valtava altistuminen, vaatteet poistetaan suihkussa lämpimällä vedellä.
Silmäkosketus
Jos ainetta joutuu silmiin, huuhtele silmät huolellisesti vedellä vähintään 15 minuutin ajan. Pidä silmäluomet auki ja poissa silmäluomista, jotta kaikki pinnat huuhdellaan huolellisesti.
Nieleminen ei ole mahdollinen altistumisreitti. Kaikissa muissa tapauksissa on saatava välitöntä lääketieteellistä apua (Praxair, 2016).
sovellukset
1- Rikin valmistus
Claus-rikin talteenottoyksikkö koostuu palamisuunista, jätelämmittimestä, rikki- lauhduttimesta ja sarjasta katalyyttisiä vaiheita, joissa kussakin käytetään kuumennus-, katalyytti- ja rikki- lauhdutinta. Tyypillisesti käytetään kahta tai kolme katalyyttistä vaihetta.
Claus-prosessi muuntaa vetysulfidin alkuaineeksi rikiksi kahden vaiheen reaktion kautta.
Ensimmäinen vaihe sisältää syöttökaasun kontrolloidun polttamisen, jotta noin kolmasosa vety- sulfidista muuttuu rikkidioksidiksi ja että ei-katalyyttistä reaktiota ei ole poltettu rikkidioksidilla.
Toisessa vaiheessa Claus-reaktio, vety- sulfidi ja rikkidioksidi reagoivat katalyytillä rikin ja veden tuottamiseksi.
Palamisilman määrää kontrolloidaan tiukasti rikin talteenoton maksimoimiseksi, eli pitämällä sopiva 2: 1-rikkivetyhapon reaktio- stoikiometria rikkidioksidiin alavirran reaktorien läpi.
Tyypillisesti voidaan saavuttaa jopa 97% rikin talteenotto (US National Library of Medicine, 2011).
2 - Analyyttinen kemia
Yli vuosisadan ajan rikkivety oli tärkeä analyyttisessä kemiassa, metalli-ionien kvalitatiivisessa epäorgaanisessa analyysissä.
Näissä analyyseissä raskasmetalli (ja ei-metalli) ionit saostetaan (esim. Pb (II), Cu (II), Hg (II), As (III) liuoksesta altistamisen jälkeen H2S: lle. Saatu sakka liukenee jälleen jonkin verran selektiivisyydellä ja siten tunnistetaan.
3 - Muut käyttötarkoitukset
Tätä yhdistettä käytetään myös erottamaan deuteriumoksidi tai raskas vesi normaalista vedestä Girdler-sulfidimenetelmän avulla.
Exeterin yliopiston tutkijat havaitsivat, että solujen altistuminen pienille määrille vety- sulfidikaasua voi estää mitokondrioiden vaurioita.
Kun solu stressaantuu taudin kanssa, entsyymit houkuttelevat soluun tuottamaan pieniä määriä vety- sulfidia. Tällä tutkimuksella voi olla enemmän vaikutuksia aivohalvausten, sydänsairauksien ja niveltulehduksen ehkäisyyn (Stampler, 2014).
Vety- sulfidilla voi olla anti-aging ominaisuuksia estämällä tuhoavia kemikaaleja solussa, joilla on samanlaiset ominaisuudet kuin resveratrolilla, antioksidantti, joka löytyy punaviinistä.
viittaukset
- Myrkyllisten aineiden ja tautien rekisterin virasto. (2011, 3. maaliskuuta). Vety- sulfidi Karbonyylisulfidi. Haettu osoitteesta atsdr.cdc.gov.
- Al-Tawfiq, B. D. (2010). Vety- sulfidialtistus aikuisilla miehillä. Annals of Saudi Med. 30 (1) , 76-80.
- EMBL-EBI. (2005, 13. joulukuuta). vetysulfidi. Palautettu osoitteesta ebi.ac.uk.
- encyclopedia britannica. (S.F.). Vety- sulfidi. Palautettu britannica.comista.
- Human Metabolome Database. (2017, 2. maaliskuuta). Vety- sulfidi . Haettu osoitteesta hmdb.ca.
- HYDROGEN SULFIDE. (2016). Haettu osoitteesta cameochemicals.noaa.gov.
- (2016, 17. lokakuuta). Vety-rikkidioksidin käyttöturvallisuustiedote. Palautettu osoitteesta praxair.com.
- Royal Society of Chemistry. (2015). Vety- sulfidi. Haettu osoitteesta chemspider.com.
- Stampler, L. (2014, 11. heinäkuuta). Stinky-yhdiste voi suojata solujen vaurioilta, opintotulokset. Haettu osoitteesta time.com.
- S. National Medicine of Medicine. (2011, 22. syyskuuta). Rikki, alkuaine. Haettu osoitteesta toxnet.nlm.nih.gov.


