Butino-rakenne, ominaisuudet ja käyttötarkoitukset
butyyni on kemiallinen yhdiste, joka kuuluu alkynien ryhmään, tunnettu siitä, että sillä on rakenne, jossa on ainakin kolme sidosta kahden hiiliatomin välillä.
Kun kyse on alkynien nimityssääntöjen laatimisesta, IUPAC (englanninkielinen lyhenne, kansainvälinen puhdas- ja sovelluskemian liitto) on osoittanut, että niitä käytetään samoin kuin alkeeneja.

Perusero molempien aineiden nimikkeistön välillä on se, että sufiksi -one muutetaan - tai kun se tulee yhdisteisiin, joilla on sen kolmessa sidoksessa oleva rakenne.
Toisaalta butino koostuu vain hiilestä ja vedystä, ja se on kahdessa muodossa: 1-butiini, joka on kaasufaasissa vakiopaine- ja lämpötilaolosuhteissa (1 atm, 25 ° C); ja 2-butino, joka on kemiallisen synteesin avulla tuotettu nestefaasilaji.
indeksi
- 1 Kemiallinen rakenne
- 1.1 1-butino
- 1.2 2-butyni
- 2 Ominaisuudet
- 3 Käyttö
- 4 Viitteet
Kemiallinen rakenne
Butinossa tunnetussa molekyylissä esitetään aseman rakenteellisen isomeroinnin ilmiö, joka koostuu samojen funktionaalisten ryhmien läsnäolosta molemmissa yhdisteissä, mutta kukin näistä on ketjun eri paikassa..
Tässä tapauksessa molemmilla butinomuodoilla on identtinen molekyylikaava; kuitenkin 1-butii- nissä kolmoissidos sijaitsee hiilen lukumäärässä yksi, kun taas 2-butyynissä se löytyy numerosta kaksi. Tämä muuntaa ne sijainnin isomeereiksi.
Kolminkertaisen sidoksen sijainnin vuoksi yhdessä 1-butyniirakenteen terminaaleista sitä pidetään terminaalisena alkeenina, kun taas kolmoissidoksen väliasento 2-butynirakenteessa antaa sille sisäisen alkynin luokituksen..
Siten linkki voi olla vain ensimmäisen ja toisen hiilen (1-butiinin) tai toisen ja kolmannen hiilen (2-butiinin) välillä. Tämä johtuu sovelletusta nimikkeistöstä, jossa pienin mahdollinen numerointi annetaan aina kolmoissidoksen asemalle.
1-butyyni
Yhdistettä, jota kutsutaan 1-butyyniksi, kutsutaan myös etyyliasetyleeniksi sen rakenteen ja sen neljän hiiliatomin järjestämisen ja sitoutumisen vuoksi. Kuitenkin, kun puhutaan butyyni viitataan vain tähän kemialliseen lajiin.
Tässä molekyylissä kolmoissidos löytyy päätehiilestä, joka sallii vetyatomien saatavuuden, joka antaa sille suuren reaktiivisuuden.
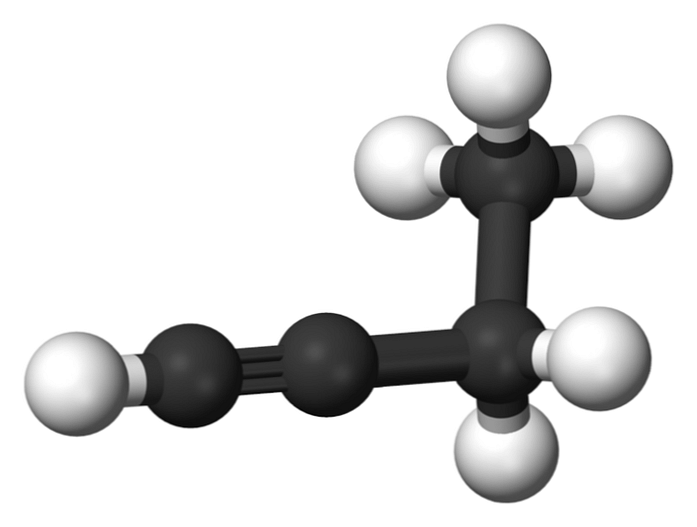
Tämä jäykkä ja voimakkaampi sidos kuin yksittäinen tai kaksoissidos hiiliatomien välillä tarjoaa stabiilin konfiguraation 1-butynin lineaariseen geometriaan.
Toisaalta tämä kaasumainen aine on varsin syttyvää, joten lämmön läsnä ollessa se voi aiheuttaa tulipaloja tai räjähdyksiä helposti ja sillä on suuri reaktiivisuus ilman tai veden läsnä ollessa.
2-butyyni
Koska sisäisillä alkyyleillä on suurempi stabiilisuus kuin terminaaliset alkyynit, ne mahdollistavat 1-butynin transformoinnin 2-butyyniksi.
Tämä isomerointi voi tapahtua kuumentamalla 1-butyniä emäksen (kuten NaOH: n, KOH: n, NaOCH3: n ...) läsnä ollessa tai järjestämällä 1-butyni uudelleen kaliumhydroksidin (KOH) liuoksessa etanolissa (C2H6O).
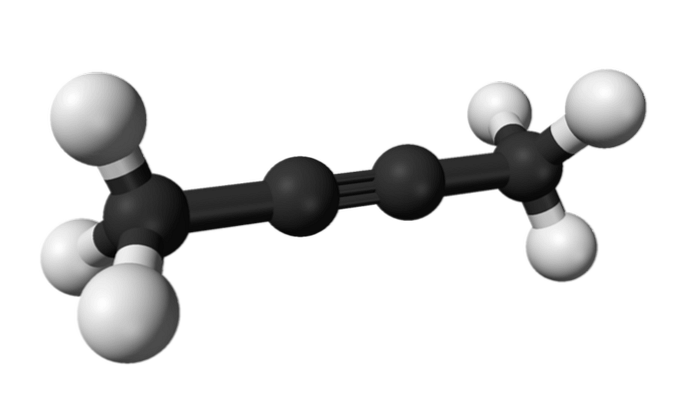
Samalla tavoin 2-butyyniksi kutsuttua kemikaalia kutsutaan myös dimetyyliaseteeniksi (tai krotonyleeniksi), joka esittää itseään nestemäisenä ja haihtuvana lajina, joka on peräisin keinotekoisesti.
2-butyliinissä kolmoissidos on molekyylin keskellä, mikä antaa sille suurempaa stabiilisuutta kuin sen isomeeri.
Lisäksi tämän värittömän yhdisteen tiheys on pienempi kuin veden, vaikka sitä pidetään liukenemattomana ja sillä on korkea syttyvyys.
ominaisuudet
-Butinon rakennekaava (riippumatta siitä, mihin isomeeriin viitataan) on C4H6, jossa on lineaarinen rakenne.
-Yksi kemiallisista reaktioista, jotka kärsivät butiinimolekyylistä, on isomerointi, jossa kolmoissidoksen uudelleenjärjestely ja siirtyminen tapahtuu molekyylissä..
-1-Butyne on kaasufaasissa, sillä on erittäin korkea syttyvyys ja suurempi tiheys kuin ilma.
-Tämä aine on myös melko reaktiivinen, ja lämmön läsnä ollessa voi aiheuttaa väkivaltaisia räjähdyksiä.
-Lisäksi kun tämä väritön kaasu palaa epätäydellisesti, se voi aiheuttaa hiilimonoksidia (CO)
-Kun molemmat isomeerit ovat alttiina korkeille lämpötiloille, ne voivat kokea räjähtäviä polymerointireaktioita.
-2-butiini on nestefaasissa, vaikka sitä pidetään myös melko syttyvänä tavanomaisissa paine- ja lämpötilaolosuhteissa.
-Näillä aineilla voi esiintyä voimakkaita reaktioita, kun ne ovat voimakkaiden hapettavien aineiden läsnä ollessa.
-Samalla tavalla eksotermiset reaktiot, joiden seurauksena vapautuu kaasumainen vety, esiintyvät, kun pelkistävien lajien läsnä ollessa..
-Kun se havaitaan kosketuksissa tiettyjen katalyyttien (kuten eräiden happamien aineiden) tai alkulajien kanssa, voi esiintyä eksotermisiä polymerointireaktioita..
sovellukset
Koska niillä on erilaisia ominaisuuksia, molemmilla isomeereillä voi olla erilaisia käyttötarkoituksia ja sovelluksia, kuten alla on esitetty:
Ensinnäkin hyvin usein yksi 1-butinon sovelluksista on sen käyttö välivaiheena muiden synteettistä alkuperää olevien orgaanisten aineiden valmistusprosessissa..
Toisaalta tätä kemiallista ainetta käytetään kumin ja siitä johdettujen yhdisteiden valmistusteollisuudessa; kuten esimerkiksi, kun haluat saada bentsolia.
Samoin sitä käytetään monenlaisten muovituotteiden valmistusprosessissa sekä monien suurtiheyksisten polyeteenien valmistuksessa..
Myös 1-butyniä käytetään usein komponenttina eräiden metalliseosten, mukaan lukien teräksen (rautaseos ja hiili) leikkaus- ja hitsausprosesseihin..
Toisessa mielessä 2-butyni-isomeeriä käytetään yhdessä toisen alkiinin kanssa, jota kutsutaan propiiniksi, joidenkin alkyloidun hydrokinonien, synteesissä, kun a-tokoferolin (E-vitamiinin) täydellinen synteesi suoritetaan.
viittaukset
- Wikipedia. (N.D.). Butyyni. Haettu osoitteesta en.wikipedia.org
- Yoder, C. H., Leber P. A. ja Thomsen, M. W. (2010). Silta orgaaniseen kemiaan: käsitteet ja nimikkeistö. Haettu osoitteesta books.google.co.ve
- Study.com. (N.D.). Butyne: rakennekaava ja isomeerit. Hankittu tutkimuksesta.
- Pubchem. (N.D.). 1-butyyni. Haettu osoitteesta pubchem.ncbi.nlm.nih.gov
- Pubchem. (N.D.). 2-butyyni. Haettu osoitteesta pubchem.ncbi.nlm.nih.gov


