Aineen (fysikaalinen ja kemiallinen) ominaispiirteet
aineen ominaispiirteet ne ovat kemiallisia tai fysikaalisia ominaisuuksia, jotka voivat auttaa tunnistamaan tai erottamaan yhden aineen toisesta. Fyysiset ominaisuudet ovat aineen ominaisuuksia, joita havaitaan aisteilla. Kemialliset ominaisuudet ovat ominaisuuksia, jotka kuvaavat, miten aine muuttuu aineesta toiseen kemiallisen reaktion aikana.
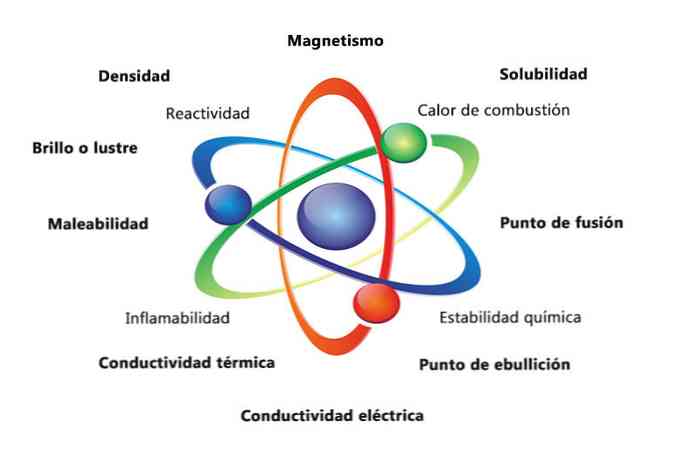
Jotkin aineen fysikaaliset ominaisuudet ovat tiheys, liukoisuus, sulamispiste, väri ja massa. Materiaalin kemialliset ominaisuudet ovat syttyvyys, reaktiivisuus happojen kanssa ja korroosio. Joitakin esimerkkejä siitä, miten aineen ominaisuudet voivat auttaa tunnistamaan elementin, on vertailla eri elementtien tiheyksiä.
Kultaisen elementin tiheys on 19,3 grammaa kuutiosenttimetriä kohden, kun taas rikin tiheys on 1,96 grammaa kuutiometriä kohti. Samoin aineiden, kuten veden ja isopropyylialkoholin, sulamispisteet ovat erilaisia.
Aineen fysikaaliset ominaisuudet
Aineen fysikaaliset ominaisuudet ovat ominaisuuksia, jotka voidaan mitata tai havaita muuttamatta aineen kemiallista luonnetta. Esimerkkejä fyysisistä ominaisuuksista ovat:
- Tiheys: kohteen sisältävän aineen määrä lasketaan jakamalla massa tilavuuden mukaan.
- Magnetismi: magneetin ja magneettisen kohteen vetovoima.
- Liukoisuus: mitataan, kuinka hyvin aine voi liueta toisessa aineessa.
- Sulamispiste: lämpötila, jossa aine muuttuu kiinteästä nesteenä.
- Kiehumispiste: lämpötila, jossa aine muuttuu nesteestä kaasuksi.
- Sähköjohtavuus: on mitta siitä, kuinka hyvin sähkövirrat liikkuvat aineen läpi.
- Lämmönjohtavuus: nopeus, jolla aine siirtää lämpöä.
- Malleability: onko aineen kyky vierittää tai jauhaa eri tavoin.
- Kiiltävä tai kiiltävä: kuinka helposti kohde heijastaa valoa.
Aineen kemialliset ominaisuudet
Kemialliset ominaisuudet kuvaavat aineen kykyä muuttaa itsestään uudeksi aineeksi, jolla on erilaiset ominaisuudet. Alla on useita esimerkkejä kemiallisista ominaisuuksista:
- Palamislämpö: energia, joka vapautuu, kun yhdiste joutuu täydelliseen polttamiseen hapella.
- Kemiallinen stabiilisuus: viittaa siihen, reagoi yhdiste veden tai ilman kanssa (kemiallisesti stabiilit aineet eivät reagoi).
- Syttyvyys: yhdisteen kyky palaa, kun se altistuu liekille.
- Reaktiivisuus: kyky toimia vuorovaikutuksessa toisen aineen kanssa ja muodostaa yhden tai useamman uuden aineen.
Aineen fyysiset tilat
Aine on mikä tahansa, joka vie tilaa, jolla on massaa ja jonka aistit voivat havaita. Aine voidaan luokitella sen fyysisen tilan mukaan: kiinteä, nestemäinen ja kaasumainen.
1 - Kiinteät aineet ja niiden ominaispiirteet
Kaikilla kiinteillä aineilla on massaa, niillä on tilaa, niillä on määrätty tilavuus ja muoto, eivät liukene avaruuden läpi eikä niitä voi puristaa tai olla jäykkiä. Meillä on esimerkkejä puusta, kirjoista, sienistä, metallista, kivistä jne..
Kiintoaineissa pienet hiukkaset ovat hyvin lähellä toisiaan ja koskettavat toisiaan. Hiukkaset ovat niin lähellä toisiaan, että ne eivät voi liikkua paljon, niiden välillä on hyvin vähän tilaa.
2- Nesteet ja niiden ominaispiirteet
Kaikilla nesteillä on massaa, niillä on tilaa, niillä on määrätty tilavuus, mutta ei määritelty muoto (koska ne sopeutuvat säiliöön, jossa ne ovat), ne voidaan puristaa hyvin pieneksi ja ne voivat liu'uttaa tilaa. Esimerkkeinä meillä on vettä, kerosiinia, öljyä jne..
Nestemäisissä aineissa pienet hiukkaset ovat hieman kauempana toisistaan, niiden välissä on enemmän tilaa (verrattuna kiintoaineisiin) ja ne eivät kosketa toisiaan. Siksi hiukkaset voivat liikkua tilojen välillä, työntämällä ja törmäämällä muiden hiukkasten kanssa, muuttamalla jatkuvasti suuntaa.
3 - Kaasut ja niiden ominaisuudet
Kaikilla kaasuilla on massaa, niillä on tilaa, niillä ei ole määritettyä tilavuutta tai muotoa, ne voidaan puristaa suuressa määrin ja voivat diffundoitua avaruuteen. Meillä on esimerkkejä: vety, happi, typpi, hiilidioksidi, höyry jne..
Kaasuissa pienet hiukkaset ovat paljon kauempana toisistaan, niiden välillä on paljon enemmän tilaa (verrattuna nesteisiin) ja ne eivät kosketa toisiaan. Hiukkasilla on maksimaalinen liikkumisvapaus, niin että ne työntävät ja törmäävät muiden hiukkasten kanssa jatkuvasti muuttuvaan suuntaan.
Aineen tilan muutokset
Aine voidaan muuntaa kiinteästä tilasta nestemäiseen tilaan ja päinvastoin ja nestemäisestä tilasta kaasumaiseen tilaan ja päinvastoin. Tämä muunnos tarkoittaa asian tilan muutosta ja tapahtuu lämpötilan muutoksilla:
fuusio
Materiaalin tilan muuttuminen kiinteästä nesteeseen lämpötilan nousun avulla. Kun kiinteää ainetta kuumennetaan, lämpö saa hiukkaset värähtelemään voimakkaammin.
Sulamispisteen saavuttamisen jälkeen kiinteillä hiukkasilla on riittävä kineettinen energia voittaakseen vetovoimat, jotka pitävät ne kiinteissä asennoissa, ja ne hajoavat muodostamaan pieniä nesteitä..
Kiehuminen tai höyrystyminen
Nestemäisen aineen tilan muuttuminen kaasumaiseksi lämpötilan nousun avulla. Kun nestemäistä ainetta kuumennetaan, lämpö saa hiukkaset liikkumaan vielä nopeammin.
Kun kiehumispiste saavutetaan, nestemäisillä hiukkasilla on riittävä kineettinen energia voittaakseen vetovoimat, jotka pitävät ne kiinteissä asennoissa, ja erottuvat yksittäisiin kaasumaisiin hiukkasiin..
Pakastaminen tai kiinteytyminen
Nestemäisen aineen tilan muuttuminen kiinteäksi lämpötilan laskun avulla. Kun nestemäinen aine jäähdytetään, sen hiukkaset menettävät paljon kineettistä energiaa. Jotta jäätymispiste saavutettaisiin, hiukkaset pysähtyvät ja värisevät kiinteässä asennossa muuttumalla kiinteiksi hiukkasiksi.
Nesteytys tai tiivistyminen
Kaasumaisen aineen tilan muuttuminen nesteenä lämpötilan laskun avulla. Kun kaasumainen aine jäähdytetään, sen hiukkaset menettävät paljon kineettistä energiaa, joka saa ne houkuttelemaan toisiaan nestemäisiksi hiukkasiksi.
sublimaatio
Jotkin materiaalit muuttuvat suoraan kiinteästä tilastaan kaasumaiseen tilaansa tai päinvastoin menemättä läpi nestemäistä tilaa. Kun näitä kiinteitä aineita kuumennetaan, niiden hiukkaset liikkuvat niin nopeasti, että ne erottavat täysin muodostavan höyryn tai kaasun, ja päinvastoin, kun prosessi tapahtuu kaasumaisesta kiinteään aineeseen.
viittaukset
- De Podesta, M. Aineen ominaisuuksien ymmärtäminen, 2. painos. Iso-Britannia: Taylor & Francis.
- Goel A. Aineiden valtiot. New Delhi: Discovery-kirjasto.
- Moore J, Stanitski C. Molekyylitiede, 5. painos. Stamford: Cengage-oppiminen.
- Ramakrishna A. Aineen luonne, 1. painos. New Delhi: Goyal Brothers Prakashan.
- Reger D, Goode S, Ball D. Kemia. Periaatteet ja käytäntö, 3. painos. Kanada: Brooks / Cole, Cengage Learning.
- Shapere D. Matter (fysiikka). Haettu osoitteesta accessscience.com.
- Singh L, Kaur M. Matter ympäristössä. Intia: S. Chand School.


