Trypanosoma brucei -ominaisuudet, morfologia, biologinen sykli, oireet
Trypanosoma brucei Se on solunulkoinen loisen alkueläin. Kuuluu Kinetoplastidae-luokkaan, Trypanosomatidae-sukuun Trypanosoma. On olemassa kaksi alalajia, jotka aiheuttavat kaksi erilaista vaihtoehtoa afrikkalaisen ihmisen trypanosomiasiksesta tai joita kutsutaan myös "unilääkkeeksi".
Trypanosoma brucei alalajia. gambiense, Länsi- ja Keski-Saharan eteläpuolisessa Afrikassa on krooninen muoto ja 98 prosenttia tapauksista. Trypanosoma brucei alalajia. rhodesiensen on Saharan eteläpuolisen Afrikan keskellä ja idässä esiintyvän akuutin muodon syy.
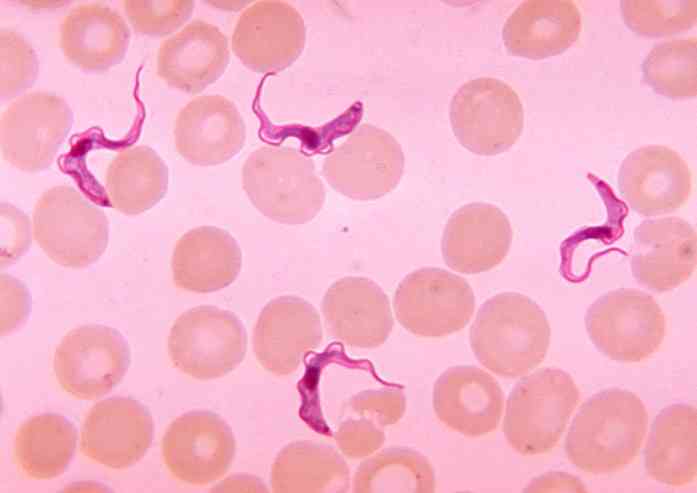
Tämän taudin molempia variantteja on raportoitu Saharan eteläpuolisen Afrikan maissa, joissa tsetse-lentää löytyy, Glossina spp, vektorin tai lähettävän aineen T. brucei.
Kolmas alalaji, Trypanosoma brucei alalajia. bruceita, samankaltainen sairaus kotieläimissä ja luonnonvaraisissa eläimissä, nimeltään nagana.
Nukkuva sairaus uhkaa yli 60 miljoonaa ihmistä 36 maassa Saharan eteläpuolisessa Afrikassa. Vuosittain on noin 300 000–500 000 tapausta, joista noin 70 000–100 000 kuolee. Tsetse-lennon saastuminen kattaa 10 miljoonan neliökilometrin alueen, joka on yksi kolmasosa Afrikan maastosta.
Maailman terveysjärjestö tunnustaa, että uusien afrikkalaisen trypanosomiasis-tapausten määrä on viime vuosina merkittävästi laskenut. Tämä johtuu kansallisista ja kansainvälisistä aloitteista tämän taudin torjumiseksi.
indeksi
- 1 Yleiset ominaisuudet
- 1.1 löytö
- 1.2 Genetics
- 1.3 "Nukkuva sairaus" ja ilmaston lämpeneminen
- 2 Fylogeny ja taksonomia
- 3 Morfologia
- 3.1 Tryomastigootti
- 3.2 Epimastigote-lomake
- 3.3 Kinetosomi
- 4 Biologinen kierros
- 4.1 Isännässä (ihminen tai muu nisäkäs)
- 4.2 Tsetse-lennossa (vektori)
- 5 Infektion oireet
- 5.1 Ensimmäinen vaihe
- 5.2 Toinen vaihe
- 5.3 Diagnoosi
- 6 Hoito
- 7 Viitteet
Yleiset ominaisuudet
Sitä kutsutaan "unihuolloksi", koska se aiheuttaa potilaan luonnollisen nukkumisjakson kääntymisen. Henkilö nukkuu päivän aikana ja pysyy hereillä yöllä. Tämä on seurausta psykologisista ja neurologisista häiriöistä, joita tauti aiheuttaa edistyneessä vaiheessa.
Löytö
Eläin- tai nagana trypanosomiasis on tärkeä sairaus Afrikassa nautaeläimillä. Hän tunnisti itsensä Trypanosoma brucei syy-agentiksi vuonna 1899. Se oli David Bruce tutkiessaan suurta Nagana-epidemiaa Zululandissa.
Myöhemmin Aldo Castellani havaitsi tämän trypanosomilajin ihmisen potilaiden veressä ja aivojen selkäydinnesteessä, jossa oli "nukkuva sairaus"..
Vuosien 1902 ja 1910 välillä tunnistettiin kaksi ihmisen taudin varianttia ja niiden aiheuttajaa. Sekä eläimet että ihmiset voivat toimia parasiittien säiliöinä, jotka kykenevät aiheuttamaan taudin ihmisellä.
genetiikka
. \ TYdin. \ T Trypanosoma brucei se koostuu 11 diploidista kromosomista ja sadasta mikrokromosomista. Yhteensä sillä on 9 068 geeniä. Mitokondrioiden genomi (kinetoplast) koostuu lukuisista pyöreän DNA: n kopioista.
"Nukkuva sairaus" ja ilmaston lämpeneminen
Afrikan ihmisen trypanosomiaasia pidetään yhtenä 12 ihmisen tartuntataudista, joita maapallon lämpeneminen voi pahentaa.
Tämä johtuu siitä, että kun ympäristön lämpötila nousee, alue, johon lento voi tarttua, laajenee. Glossina sp. Kun kolonisoimalla lentävät uudet alueet, se ottaa parasiitin mukaan.
Fylogeny ja taksonomia
Trypanosoma brucei pkuuluu valtakuntaan Protista, ryhmä Excavata, phylum Euglenozoa, luokka Kinetoplastidae, tila Trypanosomatida, perhe Trypanosomatidae, suku Trypanosoma, alalaji Tripanozoon.
Tällä lajilla on kolme alalajia, jotka aiheuttavat erilaisia "unihäiriöitä" ihmisillä (T. b. alalajia. gambiense ja T. b. subsp. Rhodesiense) sekä kotieläiminä pidetyillä ja luonnonvaraisilla \ tT. b. alalajia. bruceita).
morfologia
Tripomastigootti
Trypanosoma brucei on pitkänomainen yksisoluinen organismi, jonka pituus on 20 μm ja leveys 1-3 μm, jonka muoto, rakenne ja kalvon koostumus vaihtelevat koko elinkaarensa ajan.
Siinä on kaksi perusmuotoa. Tripomastigootti, joka muodostaa ydin- ja pitkän rungon takana olevan perusrungon muodon. Tämä lomake puolestaan edellyttää alatyyppejä elinkaaren aikana. Näistä lyhyt tai tukeva alatyyppi (slumpy englanniksi), se on paksumpi ja sen lippu on lyhyt.
Epimastigote-lomake
Toinen perusmuoto on ytimen ja rintamateriaalin etupuolella olevan peruskehon epimastigootti, joka on hieman lyhyempi kuin edellinen..
Solu peitetään vaihtelevan pinnan glykoproteiinin kerroksella. Tämä kerros muuttaa sen pinnan glykoproteiineja ja täten eliminoi isännän tuottamien vasta-aineiden hyökkäyksen.
Immuunijärjestelmä tuottaa uusia vasta-aineita, jotka hyökkäävät kerroksen uuteen kokoonpanoon ja kerros muuttuu uudelleen. Tätä kutsutaan antigeeniseksi vaihteluksi.
Kinetosoma
Tärkeä piirre on kinetosoman läsnäolo. Tämä rakenne koostuu kondensoituneesta mitokondriaalisesta DNA: sta, joka sijaitsee vain läsnä olevien mitokondrioiden sisällä. Tämä suuri mitokondriot sijaitsevat vitsauksen pohjalla.
Biologinen kierros
Elinkaaren Trypanosoma brucei vuorotellen välillä tsetse lentää vektorina ja ihmisenä isäntänä. Tällaisten erilaisten isäntien kehittymiseksi prototyyppi muuttuu merkittävistä metabolisista ja morfologisista muutoksista toiseen.
Lennossa Trypanosoma brucei asuu ruoansulatuskanavassa, kun taas ihmisessä se on veressä.
Isännässä (ihminen tai muu nisäkäs)
Trypanosoma brucei Se on kolmessa perusmuodossa koko syklin ajan. Kun lentää puree ihmisen tai muun nisäkkään veren uuttamiseksi, se pistää sylkirauhasista verenkiertoon alkueläinten ei-proliferatiivisen muodon, jota kutsutaan metasykliseksi.
Kun se on verenkierrossa, se muuttuu proliferatiiviseksi muotoksi, jota kutsutaan kapeaksi vereksi (hoikka englanniksi).
Hoikka veren muoto Trypanosoma brucei se saa energiansa veressä olevan glukoosin glykolyysistä. Tämä aineenvaihduntaprosessi tehdään glykosoomiksi kutsutulla organellilla. Nämä trypanosomit lisääntyvät eri kehon nesteissä: veressä, imusolmukkeessa ja aivo-selkäydinnesteessä.
Kun loisten määrä veressä kasvaa, ne alkavat muuttua uudelleen ei-proliferatiiviseen muotoon. Tällä kertaa se on paksumpi variantti, jossa on lyhyempi lippu, jota kutsutaan pullea vereksi (pullea).
Kupariset veripyrpanosomit on mukautettu ruuansulatuselimistön olosuhteisiin. Ne aktivoivat mitokondrioita ja entsyymejä, joita tarvitaan sitruunahappojen ja hengitysketjun sykliin. Energian lähde ei ole enää glukoosi, vaan proliini.
Lennossa tse-tsé (vektori)
Vektorin tai lähettävän aineen Trypanosoma brucei se on tse-tse lentää, Glossina spp. Tämä sukuryhmä on 25-30 hematofagisten lajien lajia. Niitä on helppo erottaa tavallisesta lennosta niiden erityisen pitkällä kouristuksella ja täysin taitetuilla siipillä levossa.
Kun tsetse-lento puree tartunnan saanutta isäntäeläintä ja purkaa veren, nämä tynkä veren muodot tunkeutuvat vektoriin.
Kerran veren ruoansulatuskanavassa tunkeutuneet verimuodot erottuvat nopeasti procyklisiksi proliferatiivisiksi trypanosomeiksi.
Ne lisääntyvät binäärisen halkeamisen avulla. He lähtevät ruoansulatuskanavasta ja menevät sylkirauhasiin. Ne muunnetaan epimastigoteiksi, jotka ankkuroituvat seiniin vitsauksen avulla.
Sylkirauhasissa ne lisääntyvät ja muuttuvat metasyklisiin trypanosomeihin, jotka ovat valmiita siirrostamaan uudelleen nisäkkään verijärjestelmään.
Infektion oireet
Tämän taudin inkubointiaika on 2 - 3 vuorokautta lento-puremisen jälkeen. Neurologiset oireet voivat ilmetä muutaman kuukauden kuluttua T. b. alalajia. gambiense. Jos se on noin T. b. alalajia. rhodesiensen, se voi kestää vuosia.
Ensimmäinen vaihe
"Nukkuva sairaus" on kaksi vaihetta. Ensimmäistä kutsutaan varhaisvaiheeksi tai hemolymfaattiseksi faasiksi, jolle on tunnusomaista läsnäolo Trypanosoma brucei vain veressä ja imusolmukkeessa.
Tällöin oireet ovat kuume, päänsärky, lihassärky, oksentelu, imusolmukkeiden turvotus, laihtuminen, heikkous ja ärtyneisyys.
Tässä vaiheessa sairaus voidaan sekoittaa malariaan.
Toinen vaihe
Ns. Myöhäisvaihe tai neurologinen vaihe (enkefaliittinen tila) aktivoituu parasiitin saapuessa keskushermostoon, joka havaitaan aivo-selkäydinnesteessä. Tällöin oireet ilmaistaan käyttäytymisen, sekaannuksen, epäjohdonmukaisuuden, unen syklin muuttumisen ja lopulta kooman muutoksina.
Taudin kehittyminen jatkuu alaryhmän osalta enintään kolmen vuoden jaksolla gambiense, päättyy kuolemaan. Kun alalaji on läsnä rhodesiensen, kuolema tulee viikkoista kuukausiin.
Niistä tapauksista, joita ei käsitelty, 100% kuolee. Myös 2-8% hoidetuista tapauksista kuolee.
diagnoosi
Diagnoosivaihe on silloin, kun veressä on infektiomuoto, nimittäin veripyrpanosomi.
Verinäytteiden mikroskooppisen tarkastelun avulla havaitaan loisen spesifinen muoto. Enkefaliittisessa vaiheessa tarvitaan selkärangan lävistys aivo-selkäydinnesteiden analysoimiseksi.
On olemassa useita molekyylitekniikoita, joilla diagnosoidaan Trypanosoma brucei.
hoito
Kapasiteetti, joka on Trypanosoma brucei muuttamalla jatkuvasti glykoproteiinien ulkokerroksen konfiguraatiota (antigeeninen vaihtelu), on hyvin vaikeaa kehittää rokotteita "nukkumistautia" vastaan..
Ei ole ennaltaehkäisevää kemoterapiaa, ja rokotetta on vähän tai ei lainkaan. Ihmisen afrikkalaisen trypanosomiasiksen neljä tärkeintä lääkettä ovat myrkyllisiä.
Melarsoprol on ainoa lääke, joka on tehokas keskushermoston sairauksien molemmille muunnoksille. On kuitenkin niin myrkyllistä, että se tappaa 5% potilaista, jotka saavat sen.
Eflornitiinia käytetään yksinään tai yhdessä nifurtimoxin kanssa yhä enenevässä määrin ensimmäisen hoitorivin avulla taudin aiheuttamalle taudille. Trypanosoma brucei alalajia. gambiense.
viittaukset
- Fenn K ja KR Matthews (2007) Trypanosoma brucei -erotuksen solubiologia. Nykyinen lausunto mikrobiologiassa. 10: 539-546.
- Fernández-Moya SM (2013) RNA: ta sitovien proteiinien RBP33: n ja DRBD3: n funktionaalinen karakterisointi geenin ilmentymisen säätelijöinä Trypanosoma brucei. ASIAKIRJA. Parasitologian ja biolääketieteen laitos "López-Neyra". Granadan toimituksellinen yliopisto, Espanja. 189 s.
- García-Salcedo JA, D Pérez-Morga, P Gijón, V Dilbeck, E Pays ja DP Nolan (2004) Actinin erilainen rooli Trypanosoma brucei -yhtiön elinkaaren aikana. EMBO Journal 23: 780-789.
- Kennedy PGE (2008) Ihmisen afrikkalaisen trypanosomiasiksen (univaikeus) jatkuva ongelma. Annals of Neurology, 64 (2), 116 - 126.
- Matthews KR (2005) Trypanosoma brucei. J. Cell Sei. 118: 283-290.
- Welburn SC, EM Fèvre, PG Coleman, M Odiit ja I Maudlin (2001) Nukkuminen: kahden sairauden tarina. TRENDIT parasitologiassa. 17 (1): 19-24.


