Kalsiumoksidin (CaO) rakenne, ominaisuudet ja käyttötavat
kalsiumoksidi (CaO) on epäorgaaninen yhdiste, joka sisältää kalsiumia ja happea ionimuodoissa (ei pidä sekoittaa kalsiumperoksidiin, CaO2). Lime on maailmanlaajuisesti tunnettu sana, joka tarkoittaa mitä tahansa epäorgaanista yhdistettä, joka sisältää karbonaatteja, kalsiumoksideja ja -hydroksideja, sekä muita metalleja, kuten piitä, alumiinia ja rautaa..
Tätä oksidia (tai kalkkia) kutsutaan myös puhekielenä kalkin tai sammutetun kalkin mukaan riippuen siitä, onko se hydratoitu. Kalkki on kalsiumoksidi, kun taas sammutettu kalkki on sen hydroksidi. Kalkkikivi (kalkkikivi tai kovettunut kalkki) puolestaan on itse asiassa sedimenttikivi, joka koostuu pääasiassa kalsiumkarbonaatista (CaCO3).

Se on yksi suurimmista luonnon kalsiumlähteistä ja muodostaa kalsiumoksidin tuotannon raaka-aineen. Miten tämä oksidi tuotetaan? Karbonaatit ovat herkkiä termiselle hajoamiselle; kuumennetaan kalsiumkarbonaatteja yli 825 ° C: n lämpötiloissa, mikä johtaa kalkin ja hiilidioksidin muodostumiseen.
Edellä esitetty lausunto voidaan kuvata seuraavasti: CaCO3(s) → CaO (t) + CO2(G). Koska maankuorella on runsaasti kalkkikiveä ja kalsiittia, ja valtamerissä ja rantoissa on runsaasti merikuoria (kalsiumoksidin tuotantoon tarkoitettuja raaka-aineita), kalsiumoksidia suhteellisen halvalla reagenssilla.
indeksi
- 1 Kaava
- 2 Rakenne
- 3 Ominaisuudet
- 3.1 Liukoisuus
- 4 Käyttö
- 4.1 Laastina
- 4.2 Lasien valmistuksessa
- 4.3 Kaivostoiminnassa
- 4.4 Silikaattiaineena
- 5 Kalsiumoksidin nanopartikkelit
- 6 Viitteet
kaava
Kalsiumoksidin kemiallinen kaava on CaO, jossa kalsium on kuin happo-ioni (elektroniseptori) Ca2+, ja happea emäksisenä ionina (elektronidonori) TAI2--.
Miksi kalsium on +2-maksu? Koska kalsium kuuluu jaksollisen taulukon ryhmään (Mr. Becambara), ja sillä on vain kaksi valenssielektronia, jotka ovat käytettävissä sidosten muodostamiseksi, jotka tuottavat happiatomin..
rakenne
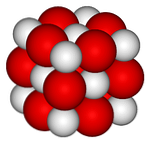
Ylemmässä kuvassa on esitetty kalsiumoksidin kiteinen rakenne (gem-salt type). Tilavat punaiset pallot vastaavat Ca-ioneja2+ ja valkoiset pallot ioneihin O2-.
Tässä kuutio- kiteisessä järjestelyssä kukin ioni Ca2+ ympäröi kuusi ionia O2-, suljettu suurten ionien jättämien oktaedristen reikien väliin.
Tämä rakenne ilmaisee tämän oksidin ionisen luonteen, vaikka säteiden huomattava ero (punainen pallo on suurempi kuin valkoinen) antaa heikomman kiteisen retikulaarisen energian verrattuna MgO: iin..
ominaisuudet
Fyysisesti se on kiteistä valkoista kiinteää ainetta, joka on hajuton ja jolla on voimakkaat sähköstaattiset yhteisvaikutukset ja jotka ovat vastuussa sen korkeasta sulamispisteestä (2572 ° C) ja kiehumispisteestä (2850 ° C). Lisäksi sen molekyylipaino on 55 958 g / mol ja mielenkiintoinen ominaisuus on termoluminesenssi.
Tämä tarkoittaa sitä, että liekkiin altistettu kalsiumoksidi palaa voimakkaalla valkoisella valolla, joka tunnetaan englanniksi ja jonka nimi on parrasvalot, tai espanjaksi, kalsiumin valo. Ca-ionit2+, tulipalon kanssa, ne aiheuttavat punertavan liekin, kuten seuraavassa kuvassa on esitetty.

liukoisuus
CaO on emäksinen oksidi, jolla on voimakas affiniteetti veteen siinä määrin, että se imee kosteutta (se on hygroskooppinen kiinteä aine), joka reagoi välittömästi sammutetun kalkin tai kalsiumhydroksidin tuottamiseen:
CaO (t) + H2O (l) => Ca (OH)2(S)
Tämä reaktio on eksoterminen (vapauttaa lämpöä) johtuen kiinteän aineen muodostumisesta vahvemmilla vuorovaikutuksilla ja stabiililla kristalliristikolla. Reaktio on kuitenkin palautuva, jos Ca (OH) kuumennetaan2, dehydratoidaan ja valaistu sammutettu kalkki; sitten kalkki "uudestisyntynyt".
Tuloksena oleva liuos on hyvin emäksinen, ja jos se on kyllästetty kalsiumoksidilla, se saavuttaa pH: n 12,8.
Samoin se liukenee glyseroliin ja happo- ja sokeriliuoksiin. Koska se on emäksinen oksidi, sillä on luonnollisesti tehokas vuorovaikutus happooksidien (SiO) kanssa2, että2O3 ja usko2O3, esimerkiksi) on liukoinen sen nestefaaseihin. Toisaalta se ei liukene alkoholeihin ja orgaanisiin liuottimiin.
sovellukset
CaO: lla on suuri määrä teollisia käyttötarkoituksia sekä asetyleenin synteesissä (CH≡CH) fosfaattien uuttamisessa jätevesistä ja reaktiossa rikkidioksidin kanssa kaasumaisista jätteistä..
Muita kalsiumoksidin käyttötarkoituksia kuvataan seuraavassa:
Laastina
Jos kalsiumoksidi sekoitetaan hiekkaan (SiO2) ja vesi, kakut hiekalla ja reagoi hitaasti veden kanssa muodostaen sammutettua kalkkia. CO2 ilmasta liukenee veteen ja reagoi suolan kanssa kalsiumkarbonaatin muodostamiseksi:
Ca (OH)2(s) + CO2(g) => CaCO3(s) + H2O (l)
CaCO3 Se on vastustuskykyisempi ja kovempi yhdiste kuin CaO, jolloin laasti (edellinen seos) kovettuu ja kiinnittää tiilet, lohkot tai keramiikka niiden välillä tai haluttuun pintaan.
Lasien valmistuksessa
Lasien valmistuksessa olennainen raaka-aine on piioksidit, jotka sekoitetaan kalkin, natriumkarbonaatin (Na2CO3) ja muut lisäaineet kuumennetaan, jolloin saadaan lasimainen kiinteä aine. Tämä kiinteä aine kuumennetaan ja puhalletaan minkä tahansa kuvion mukaan.
Kaivostoiminnassa
Haihtunut kalkki on suurempi kuin kalkki, mikä johtuu vetyliitoksen (O-H-O) vuorovaikutuksista. Tätä ominaisuutta käytetään murtamaan kivet sisältä.
Tämä saavutetaan täyttämällä ne kompaktien kalkin ja veden seoksella, joka suljetaan siten, että se keskittyy lämmön ja ekspansiivisen voiman kalliin.
Silikaattipoistajana
CaO sulatetaan silikaattien kanssa muodostamaan koalesoiva neste, joka sitten uutetaan tietyn tuotteen raaka-aineesta.
Esimerkiksi rautamalmit ovat raaka-aine metallisen raudan ja teräksen tuotannossa. Nämä mineraalit sisältävät silikaatteja, jotka ovat epätoivottuja epäpuhtauksia prosessille ja jotka poistetaan juuri kuvatulla menetelmällä.
Kalsiumoksidin nanopartikkelit
Kalsiumoksidi voidaan syntetisoida nanopartikkeleina, mikä muuttaa kalsiumnitraatin pitoisuuksia (Ca (NO)3)2) ja natriumhydroksidia (NaOH) liuoksessa.
Nämä hiukkaset ovat pallomaisia, emäksisiä (samoin kuin makro- asteikko) ja niillä on paljon pinta-alaa. Näin ollen nämä ominaisuudet hyödyttävät katalyyttisiä prosesseja. Mitä? Tutkimukset vastaavat tällä hetkellä tähän kysymykseen.
Näitä nanohiukkasia on käytetty syntetisoimaan pyridiinistä johdettuja substituoituja orgaanisia yhdisteitä uusien lääkkeiden formuloimiseksi kemiallisten transformaatioiden, kuten keinotekoisen fotosynteesin, suorittamiseksi veden puhdistamiseksi raskaista ja myrkyllisistä metalleista, ja fotokatalyyttiset aineet.
Nanohiukkaset voidaan syntetisoida biologiselle alustalle, kuten papaijan ja vihreän teen lehdille, joita käytetään antibakteerisena aineena.
viittaukset
- scifun.org. (2018). Kalkki: kalsiumoksidi. Haettu 30. maaliskuuta 2018 osoitteesta: scifun.org.
- Wikipedia. (2018). Kalsiumoksidi. Haettu 30. maaliskuuta 2018 osoitteesta: en.wikipedia.org
- Ashwini Anantharaman et ai. (2016). Kalsiumoksidi-nanohiukkasten ja sen sovellusten vihreä synteesi. Int. Journal of Engineering Research and Application. ISSN: 2248-9622, osa 6, numero 10, (osa -1), s. 27-31.
- J. Safaei-Ghomi et ai. (2013). Kalsiumoksidi-nanohiukkaset katalysoivat yksivaiheisen monikomponenttisen erittäin substituoitujen pyridiinien synteesin vesipitoisessa etanoliväliaineessa Scientia Iranica, transaktiot C: kemian ja kemian tekniikka.
- Pubchem. (2018). Kalsiumoksidi. Haettu 30. maaliskuuta 2018 osoitteesta: pubchem.ncbi.nlm.nih.gov
- Shiver & Atkins. (2008). Epäorgaaninen kemia sisään Ryhmän 2 elementit. (neljäs painos, sivu 280). Mc Graw Hill.


