Kemiallinen hybridisaatio sp, sp2, sp3
kemiallinen hybridisaatio on atomi-orbitaalien "seos", jonka käsite otti käyttöön kemisti Linus Pauling vuonna 1931 Valencian linkin teorian (TEV) puutteiden kattamiseksi. Mitä puutteita? Nämä ovat: molekyylien geometria ja vastaava linkin pituus molekyyleissä, kuten metaanissa (CH4).
TEV: n mukaan metaanissa C: n atomi-orbitaalit muodostavat neljä σ-sidosta neljän H-atomin kanssa, ja 2p: n orbitaalit, joiden muodot ovat C: n alareunassa, ovat kohtisuorassa toisiinsa nähden, joten H: t tulisi erottaa toisistaan toiset 90 asteen kulmassa.
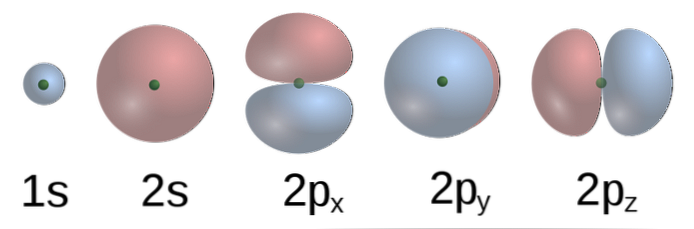
Lisäksi C: n 2s (pallomainen) orbitaali on kytketty H: n 1s-orbitaaliin 135 °: n kulmassa muihin kolmeen H: een nähden, mutta on kokeellisesti havaittu, että kulmat CH-alueella4 ovat 109,5º ja lisäksi C-H-sidosten pituudet ovat vastaavia.
Tämän selittämiseksi on katsottava, että yhdistelmä alkuperäisistä atomisista orbitaaleista muodostaa neljä degeneroitua hybridi-orbitaalia (yhtä energiaa). Tässä on kemiallinen kemia. Mitkä ovat hybridi-orbitaalit? Se riippuu niiden muodostavista atomi-orbitaaleista. Niissä on myös näiden elektronisten ominaisuuksien yhdistelmä.
indeksi
- 1 sp3 Hybridisaatio
- 1.1 Tulkkaus
- 1.2 Linkkien kulmien poikkeamat
- 2 Hybridisaatio sp2
- 3 Hybridisaatio sp
- 4 Viitteet
Hybridisaatio sp3
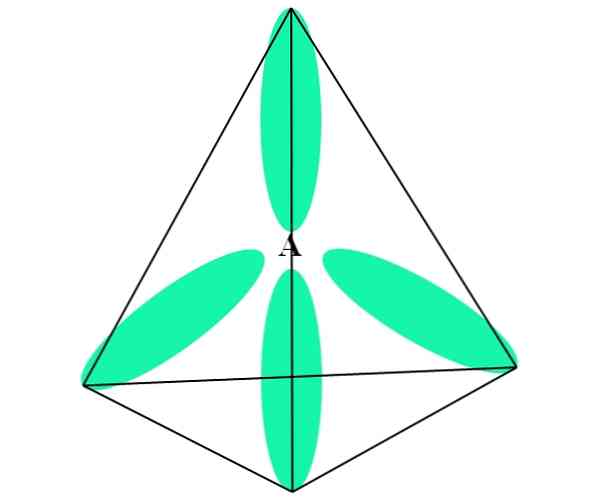
CH: n tapauksessa4, C: n hybridisaatio on sp3. Tästä lähestymistavasta molekyyli- geometria selitetään neljällä sp orbitaalilla3 erotettu 109,5º: ssa ja osoittaa kohti tetraedronin pisteitä.
Yllä olevassa kuvassa näet miten sp orbitaalit3 (vihreä) muodostavat tetraedrisen sähköisen ympäristön atomin ympärille (A, joka on C CH: lle4).
Miksi 109,5º ja ei muita kulmia, jotta "piirrettäisiin" eri geometria? Syynä tähän on se, että tämä kulma minimoi neljän atomin, jotka on liitetty A: hen, sähköiset kumoukset.
Tällä tavalla CH-molekyyli4 voidaan esittää tetraedronina (tetraedrinen molekyyli- geometria).
Jos H: n sijaan C muodostaisi yhteyksiä muihin atomiryhmiin, mikä olisi sen hybridisaatio? Niin kauan kuin hiili muodostaa neljä σ-sidosta (C-A), sen hybridisaatio on3.
Voidaan olettaa, että muissa orgaanisissa yhdisteissä, kuten CH3OH, CCl4, C (CH3)4, C6H12 (sykloheksaani), jne., hiilellä on sp-hybridisaatio3.
Tämä on välttämätöntä luonnostaan orgaanisia rakenteita, joissa hiilit, joissa on yksinkertaiset sidokset, edustavat eroja; eli rakenne ei pysy yhdessä tasossa.
tulkinta
Mikä on näiden hybridi-orbitaalien yksinkertaisin tulkinta käsittelemättä matemaattisia näkökohtia (aaltofunktioita)? Sp orbitaalit3 merkitsevät, että ne ovat peräisin neljästä kiertoradasta: yksi s ja kolme p.
Koska näiden atomi-orbitaalien yhdistelmän on tarkoitus olla ihanteellinen, neljä sp orbitaalia3 tuloksena ovat identtiset ja niissä on eri suunnat avaruudessa (kuten orbitaaleissax, pja ja pz).
Edellä mainittu on sovellettavissa muuhun mahdolliseen hybridisaatioon: muodostuneiden hybridi-orbitaalien lukumäärä on sama kuin yhdistetyissä atomirakeissa. Esimerkiksi sp-hybridipallot3d2 ne on muodostettu kuudesta atomipallosta: yksi s, kolme p ja kaksi d.
Linkkien kulmien poikkeamat
Valencian kerroksen (VSEPR) elektronisten parien repulsion teorian mukaan vapaan elektronin pari vie enemmän tilavuutta kuin linkitetty atomi. Tämä saa linkit liikkumaan toisistaan, vähentäen elektronista jännitettä ja ohjaamalla 109,5º: n kulmat:
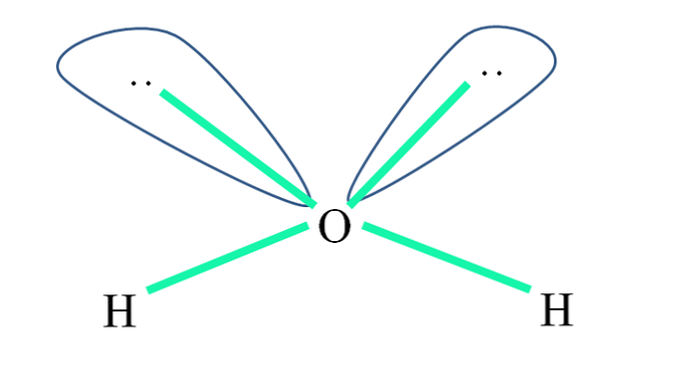
Esimerkiksi vesimolekyylissä H-atomit ovat sitoutuneet sp orbitaaleihin3 (vihreänä), ja myös elektronien parit, jotka eivät ole jaettuja ":" vievät nämä orbitaalit.
Näiden elektronien parien repulsiot ovat yleensä edustettuina "kahdella pallolla silmillä", jotka niiden tilavuuden takia kumoavat kaksi sidosta σ O-H.
Niinpä vedessä linkkien kulmat ovat todella 105º, sen sijaan että ne ovat tetraedrisen geometrian odotettua 109,5º.
Mitä geometriaa H on?2O? Siinä on kulma-geometria. Miksi? Koska vaikka elektroninen geometria on tetraedrinen, kaksi paria ei-jaettua elektronia heikentävät sitä kulmamolekyyliseen geometriaan.
Hybridisaatio sp2
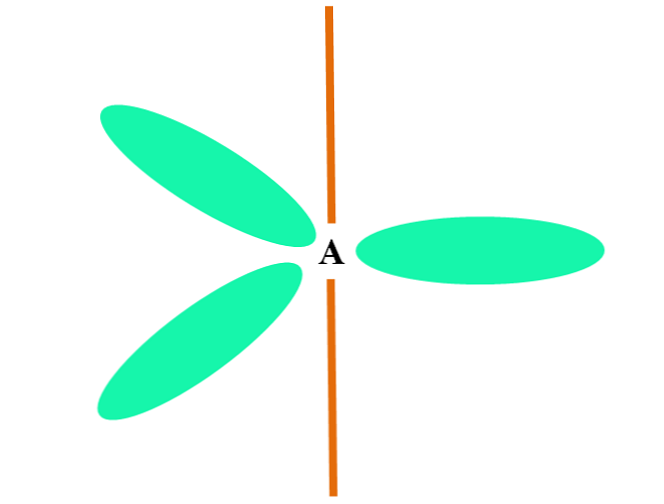
Kun atomi yhdistää kaksi p: n ja yhden orbitaalia, se tuottaa kolme sp-hybridi-orbitaalia2; Orbitaali p pysyy kuitenkin muuttumattomana (koska ne ovat kolme), joka on esitetty oranssina palkkina yllä olevassa kuvassa.
Tässä kolme sp orbitaalia2 ne ovat vihreitä korostaakseen eronsa oranssista palkista: "puhdas" p orbitaali.
Atomi, jolla on sp-hybridisaatio2 voidaan visualisoida tasaisena kolmiulotteisena kerroksena (kolmio, joka on piirretty sp orbitaaleilla2 vihreällä värillä), sen pisteet erotetaan 120º kulmilla ja kohtisuorassa baariin nähden.
Mitä roolia puhtaalla p-radalla on? Se, että muodostetaan kaksoissidos (=). Sp orbitaalit2 sallia kolmen σ-sidoksen muodostuminen, kun taas puhdas p-orbitaali on π-sidos (kaksinkertainen tai kolmoissidos merkitsee yhtä tai kahta π-sidosta).
Esimerkiksi karbonyyliryhmän ja formaldehydimolekyylin rakenteen (H2C = O), tapahtuu seuraavasti:
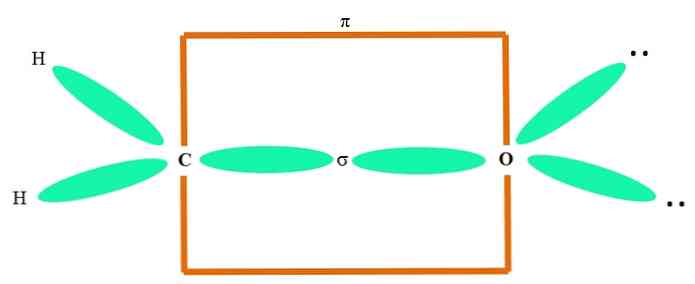
Sp orbitaalit2 sekä C että O muodostavat sidoksen σ, kun taas niiden puhtaat orbitaalit muodostavat sidoksen π (oranssi suorakulmio).
Voidaan nähdä, miten muut elektroniset ryhmät (H-atomit ja ei-jaetut elektroniparit) sijaitsevat muissa sp orbitaaleissa.2, 120 °.
Hybridisaatio sp
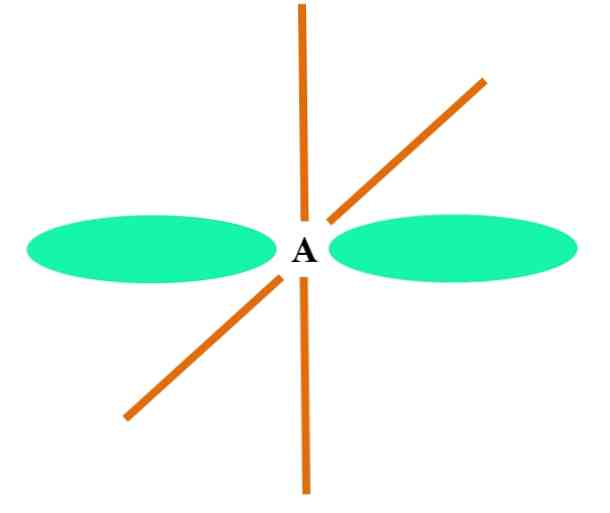
Ylempi kuva esittää atomia A sp-hybridisaatiolla. Tässä orbitaali s ja p orbitaali muodostavat kaksi degeneroitua sp orbitaalia. Nyt kaksi puhdasta p orbitaalia pysyvät kuitenkin ennallaan, mikä mahdollistaa A: n muodostavan kaksi kaksoissidosta tai kolmoissidoksen (().
Toisin sanoen: jos rakenteessa C täyttää edellä mainitut (= C = tai C = C), sen hybridisaatio on sp. Muille vähemmän havainnollisille atomeille, kuten siirtymämetalleille, elektronisten ja molekyylien geometrian kuvaus on monimutkainen, koska myös orbitaalien d ja jopa f orbitaalit otetaan huomioon..
Hybridi-orbitaalit erotetaan 180 asteen kulmassa. Tästä syystä linkitetyt atomit on järjestetty lineaariseen molekyylipainoon (B-A-B). Lopuksi alla olevassa kuvassa näet syanidianionin rakenteen:

viittaukset
- Sven. (3. kesäkuuta 2006). S-p-orbitaalit. [Kuva]. Haettu 24. toukokuuta 2018 alkaen: commons.wikimedia.org
- Richard C. Banks. (Toukokuu 2002). Liimaus ja hybridisaatio. Haettu 24. toukokuuta 2018 osoitteesta: chemistry.boisestate.edu
- James. (2018). Hybridisaatio-pikakuvake. Haettu 24. toukokuuta 2018 alkaen: masterorganicchemistry.com
- Tohtori Ian Hunt. Kemian laitos, Calgaryn yliopisto. sp3-hybridisaatio. Haettu 24. toukokuuta 2018 osoitteesta: chem.ucalgary.ca
- Kemiallinen sitominen II: Molekyyligeometria ja atomirakeiden hybridisaatio Luku 10. [PDF]. Haettu 24. toukokuuta 2018 osoitteesta: wou.edu
- Quimitube. (2015). Kovalenttinen sidos: Johdatus atomirakeiden hybridisaatioon. Haettu 24. toukokuuta 2018 alkaen: quimitube.com
- Shiver & Atkins. (2008). Epäorgaaninen kemia (Neljäs painos, sivu 51). Mc Graw Hill.


