Valenssikerros, mitä se koostuu, esimerkkejä
valenssi on sellainen, jonka elektronit ovat vastuussa elementin kemiallisista ominaisuuksista. Tämän kerroksen elektronit ovat vuorovaikutuksessa naapuriatomin kanssa, jolloin muodostuu kovalenttisia sidoksia (A-B); ja jos ne kulkevat yhdestä atomista toiseen enemmän elektronegatiivisiin, ionisiin sidoksiin (A + B-).
Tämä kerros määritellään pää kvanttiluvulla n, joka puolestaan osoittaa ajanjakson, jossa elementti on jaksollisessa taulukossa. Vaikka ryhmien tilaaminen riippuu valenssikerroksessa kiertävien elektronien lukumäärästä. Joten a n 2, voi olla kahdeksan elektronia: kahdeksan ryhmää (1-8).
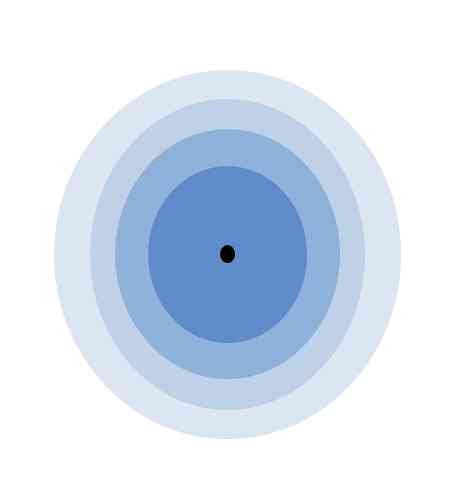
Valenssikerroksen merkitys on esitetty ylemmässä kuvassa. Atomin keskellä oleva musta piste on ydin, kun taas loput samankeskiset ympyrät ovat elektronisia kerroksia, jotka on määritelty n.
Kuinka monta kerrosta tämä atomi on? Jokaisella heistä on oma värinsä ja neljä, sitten atomissa on neljä kerrosta (n= 4). Huomaa myös, että väri hajoaa, kun etäisyys kerroksesta ytimeen kasvaa. Valenssikerros on se, joka on kauimpana ytimestä: kevyin väri.
indeksi
- 1 Mikä on Valencian taso?
- 2 Ominaisuudet
- 3 Esimerkkejä
- 3.1 Esimerkki 1
- 3.2 Esimerkki 2
- 4 Viitteet
Mikä on Valencian taso?
Kuvan mukaan valenssikuori ei ole mitään muuta kuin elektronien viimeisimpiä orbitaaleja. Vaaleansinisessä kerroksessa n= 4, on sarja 4s, 4p, 4d ja 4f orbitaaleja; toisin sanoen sisällä on muita alikerroksia, joilla on erilaiset elektroniset ominaisuudet.
Atomi tarvitsee elektroneja täyttääkseen kaikki 4n orbitaalit. Tämä prosessi voidaan havaita elementtien elektronisissa konfiguraatioissa tietyn ajan kuluessa.
Esimerkiksi kaliumilla on elektroninen konfiguraatio [Ar] 4s1, kalsium, oikealla, [Ar] 4s2. Mikä on näiden kokoonpanojen mukaan valenssikerros? Termi [Ar] viittaa jalokaasun argonin 1: n elektroniseen kokoonpanoon22s22p63S23p6. Tämä edustaa sisäistä tai suljettua kerrosta (joka tunnetaan myös nimellä ydin).
Koska 4s-kiertorata on se, jolla on korkein energia ja jossa uudet elektronit tulevat sisään, se edustaa sekä K: n että Ca: n valenssikerrosta. Jos K: n ja Ca: n atomeja verrattiin kuvassa olevaan, [Ar] olisi kaikki siniset sisäkerrokset; ja 4s on vaaleansininen kerros, ulompi.
piirteet
Kaikista edellä mainituista voidaan tiivistää joitakin valenssikerroksen ominaisuuksia kaikille atomeille:
-Energian tasosi on korkeampi; joka on sama, poistetaan enemmän ytimestä ja sillä on pienin elektroninen tiheys (verrattuna muihin kerroksiin).
-Se on epätäydellinen. Siksi se on edelleen täynnä elektroneja, kun käydään läpi ajanjakson taulukossa vasemmalta oikealle.
-Osallistuu kovalenttisten tai ionisten sidosten muodostumiseen.
Metallien ja kaliumin osalta ne hapetetaan kationeiksi. K+ sillä on elektroninen konfiguraatio [Ar], koska se menettää ainoat ulkoiset elektroninsä 4: t1. Ja Ca: n puolella2+, sen konfiguraatio on myös [Ar]; koska elektronin menettämisen sijaan menetät kaksi (4s2).
Mutta mikä on ero K: n välillä+ ja Ca2+, jos molemmat menettävät valenssikuorensa elektronit ja niillä on elektroninen konfiguraatio [Ar]? Ero on niiden ionisäteissä. ca2+ on pienempi kuin K+, koska kalsiumiatomilla on ylimääräinen protoni, joka houkuttelee voimakkaammin ulkoisia elektroneja (suljettuja tai valenssikerroksia).
4s-valenssikerros ei ole hävinnyt: se on vain tyhjä näille ioneille.
esimerkit
Valenssikerroksen käsite löytyy suoraan tai epäsuorasti useista kemian osa-alueista. Koska niiden elektronit ovat sellaisia, jotka osallistuvat linkkien muodostumiseen, kaikki niihin kohdistuvat aiheet (TEV, VSRP, reaktiomekanismit jne.) On viitattava kyseiseen kerrokseen.
Tämä johtuu siitä, että tärkeämpi kuin valenssikerros ovat sen elektronit; nimeltään valenssielektronit. Kun ne esitetään elektronisten kokoonpanojen asteittaisessa rakentamisessa, ne määrittävät atomin elektronisen rakenteen ja siten sen kemialliset ominaisuudet.
Tämän atomin A ja toisen B informaation perusteella niiden yhdisteiden rakenteet voidaan piirtää Lewis-rakenteiden läpi. Voit myös määrittää joukon yhdisteiden elektronisia ja molekyylirakenteita valenssielektronien määrän ansiosta.
Mahdolliset ja yksinkertaisimmat esimerkit valenssikerroksista löytyvät jaksollisesta taulukosta; erityisesti sähköisissä kokoonpanoissa.
Esimerkki 1
On mahdollista tunnistaa elementti ja sen sijainti jaksollisessa taulukossa vain elektronisella konfiguraatiolla. Joten jos X-elementillä on konfiguraatio [Kr] 5s25p1, Mitä se on ja mihin ajanjaksoon ja ryhmään se kuuluu??
sillä n= 5, X on viidennessä jaksossa. Lisäksi siinä on kolme valenssielektronia: kaksi 5s: n kiertoradalla2 ja yksi 5p: ssä1. Sisäinen kerros [Kr] ei anna lisätietoja.
Koska X: llä on kolme elektronia, ja sen 5p-rungot ovat epätäydellisiä, se on p-lohkossa; Lisäksi ryhmässä IIIA (romaaninen järjestelmä) tai 13 (nykyinen numerointijärjestelmä, jonka IUPAC on hyväksynyt). X on sitten intialainen elementti, In.
Esimerkki 2
Mikä on X-elementti, jossa on elektroninen kokoonpano [Kr] 4d105S1? Huomaa, että kuten In, se kuuluu jaksoon 5, koska 5s: n kiertorata1 Se on suurin energia. Valenssikerros sisältää kuitenkin myös 4d-orbitaalit, koska ne ovat epätäydellinen.
Valenssikerrokset voidaan sitten nimetä nsnp: ksi lohkon p tai s elementin suhteen; tai (n-1) dns lohkon d elementille. Niinpä salaperäinen elementti X kuuluu lohkoon d, koska sen elektroninen kokoonpano on tyyppiä (n-1) dns (4d105S1).
Mikä ryhmä kuuluu? 4d: n orbitaalin kymmenen elektronin lisääminen10, ja yksi viidestä1, X: llä on yksitoista valenssielektronia. Siksi sen on sijaittava ryhmässä IB tai 11. Siirtyminen sitten jaksollisen taulukon jaksolle 5 ryhmään 11, hopeaelementti kohdataan, Ag.
viittaukset
- Shiver & Atkins. (2008). Epäorgaaninen kemia (neljäs painos, sivu 23). Mc Graw Hill.
- Whitten, Davis, Peck & Stanley. Kemia. (8. painos). CENGAGE Learning, s. 287.
- NDT-resurssikeskus. (N.D.). Valence Shell. Otettu: nde-ed.org
- Clackamas Community College. (2002). Valence Electronit. Haettu osoitteesta dl.clackamas.edu
- Kemia LibreTexts. (N.D.). Valence ja Core Electronit. Haettu osoitteesta: chem.libretexts.org


