Kalorimetrin historia, osat, tyypit ja niiden ominaisuudet
kalorimetri on laite, jota käytetään mittaamaan lämpötilan muutosta tietyn ominaislämmön aineen (tavallisesti veden) määrässä. Tämä lämpötilan muutos johtuu tutkittavassa prosessissa absorboituneesta tai vapautuneesta lämmöstä; kemiallinen, jos se on reaktio, tai fyysinen, jos se koostuu vaiheesta tai tilamuutoksesta.
Laboratoriossa yksinkertaisin kalorimetri löytyy kahvikupista. Sitä käytetään mittaamaan lämpöä, joka on absorboitunut tai vapautunut reaktiossa vakiopaineessa vesiliuoksessa. Reaktiot valitaan välttämään reagenssien tai kaasumaisia tuotteita.
 Eksotermisessä reaktiossa vapautuvan lämmön määrä voidaan laskea kalorimetrin ja vesiliuoksen lämpötilan noususta:
Eksotermisessä reaktiossa vapautuvan lämmön määrä voidaan laskea kalorimetrin ja vesiliuoksen lämpötilan noususta:
Reaktiossa vapautuva lämmön määrä = kalorimetrin absorboima lämpö + liuoksen absorboima lämmön määrä
Kalorimetrin absorboiman lämmön määrää kutsutaan kalorimetrin kalorikapasiteetiksi. Tämä määritetään syöttämällä tunnettu määrä lämpöä kalorimetrille, jolla on tietty vesimäärä. Sitten mitataan kalorimetrin ja sen sisältämän liuoksen lämpötilan nousu.
Näiden tietojen ja veden ominaislämmön käytön (4,18 J / g.ºC) avulla voidaan laskea kalorimetrin kalorikapasiteetti. Tätä kapasiteettia kutsutaan myös kalorimetriksi.
Toisaalta vesiliuoksella saatu lämpö on yhtä suuri kuin m · ce · Δt. Kaavassa m = veden massa, ce = veden erityinen lämpö ja Δt = lämpötilan vaihtelu. Kaiken tämän perusteella voidaan laskea eksotermisen reaktion vapauttaman lämmön määrä.
indeksi
- 1 Kalorimetrin historia
- 2 osaa
- 3 Tyypit ja niiden ominaisuudet
- 3.1 Kahvikuppi
- 3.2 Kalorimetrinen pumppu
- 3.3 Adiabaattinen kalorimetri
- 3.4 Isoperibolinen kalorimetri
- 3.5 Virtauskalorimetri
- 3.6 Kalorimetri differentiaalista skannauskalorimetriaa varten
- 4 Sovellukset
- 4.1 Fysikokemiassa
- 4.2 Biologisissa järjestelmissä
- 4.3 Happipumpun ja kalorien teho
- 5 Viitteet
Kalorimetrin historia
Vuonna 1780 Ranskan apteekki A. L. Lavoisier, jota pidettiin yhtenä kemian isänä, käytti merisikaa mittaamaan lämpötuotantoa hengittämällä.
Miten? Kalorimetrin kaltaisen laitteen käyttäminen. Marsujen tuottama lämpö osoitti laitteen ympäröivän lumen sulamisen.
Tutkijat A. L Lavoisier (1743-1794) ja P. S. Laplace (1749-1827) suunnittelivat kalorimetrin, jota käytettiin ruumiin ominaislämmön mittaamiseen jään sulamismenetelmällä..
Kalorimetri koostui tinauksesta päällystetystä lieriömäisestä dekantterilasista, lakattu, kolmijalkainen ja sisäisesti päätetty suppilolla. Sisällä toinen lasi asetettiin samanlaiseen tapaan kuin edellinen, jossa oli ulkokammion läpi kulkeva putki, joka oli varustettu avaimella. Toisen lasin sisällä oli ruudukko.
Tässä ruudussa asetettiin olento tai esine, jonka erityistä lämpöä haluttiin määrittää. Jää asetettiin samankeskisten alusten sisään, aivan kuten korissa.
Jään tuottama lämpö imeytyi, mikä aiheutti sen fuusion. Ja jään sulamisen nestemäinen vesituote kerättiin avaamalla sisemmän lasin avain.
Ja lopuksi, punnittiin vettä, sulan jään massa oli tiedossa.
osat
Kemian opetuslaboratorioiden yleisimmin käytetty kalorimetri on ns. Kahvikupin kalorimetri. Tämä kalorimetri koostuu dekantterilasista tai sen sijaan anime- materiaalista, jossa on tiettyjä eristysominaisuuksia. Tässä säiliössä vesiliuos sijoitetaan kehoon, joka tuottaa tai absorboi lämpöä.
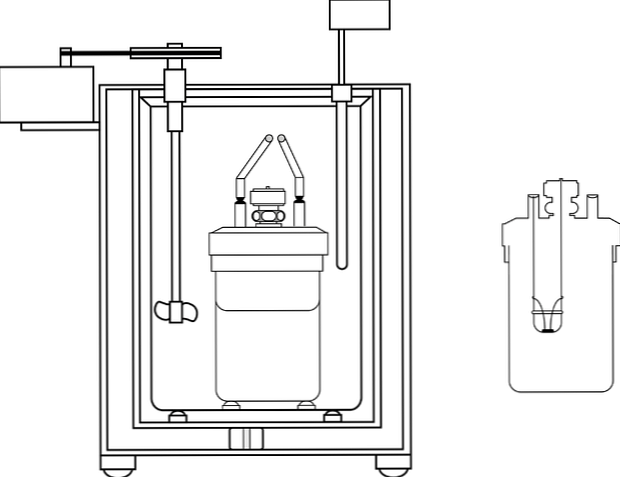
Säiliön yläosassa on eristysmateriaalin kansi, jossa on kaksi reikää. Yhdessä lämpömittari lisätään lämpötilan muutosten mittaamiseen ja toisessa sekoittimessa, edullisesti lasimateriaalissa, joka suorittaa vesiliuoksen sisällön siirtämisen..
Kuvassa on kalorimetrisen pumpun osat; On kuitenkin havaittavissa, että siinä on lämpömittari ja sekoitin, yhteiset elementit useissa kalorimetreissä.
Tyypit ja niiden ominaisuudet
Kahvikuppi
Se on sellainen, jota käytetään eksotermisen reaktion vapauttaman lämmön määrittämisessä, ja endotermisessä reaktiossa absorboitunut lämpö.
Lisäksi sitä voidaan käyttää kehon ominaislämmön määrittämiseen; toisin sanoen lämmön määrä, jonka aineen gramman täytyy absorboida sen lämpötilan nostamiseksi yhdellä celsiusasteella. .
Kalorimetrinen pumppu
Se on laite, jossa mitataan lämpöä, joka vapautuu tai absorboi reaktiossa, joka esiintyy vakio- tilavuudessa.
Reaktio tapahtuu vahvassa teräsastiassa (pumpussa), joka upotetaan suureen tilavuuteen vettä. Tämä tekee veden lämpötilan muutoksista pieniä. Siksi oletetaan, että reaktioon liittyvät muutokset mitataan vakiolämpötilassa ja tilavuudessa.
Edellä esitetty osoittaa, että työtä ei suoriteta, kun reaktio suoritetaan kalorimetrisessä pumpussa.
Reaktio alkaa syöttämällä sähköä pumppuihin liitettyjen kaapeleiden kautta.
Adiabaattinen kalorimetri
Sille on tunnusomaista, että sillä on eristysrakenne, jota kutsutaan suojaksi. Suojus sijaitsee solun ympärillä, jossa esiintyy lämpö- ja lämpötilamuutoksia. Se on myös kytketty sähköiseen järjestelmään, joka pitää lämpötilansa hyvin lähellä solun lämpötilaa lämmönsiirron välttämiseksi.
Adiabaattisessa kalorimetrissä kalorimetrin ja sen ympäristön lämpötilaero on minimoitu; sekä minimoida lämmönsiirtokerroin ja lämmönvaihtoaika.
Sen osat koostuvat seuraavista:
-Kenno (tai säiliö), joka on integroitu eristysjärjestelmään, jonka avulla yritetään välttää lämpöhäviöitä.
-Lämpömittari mittaa lämpötilan muutoksia.
-Lämmitin, joka on kytketty ohjattavaan sähköjännitteeseen.
-Ja kilpi, jo mainittiin.
Tämäntyyppisessä kalorimetrissä voidaan määrittää sellaisia ominaisuuksia kuin entropia, Debye-lämpötila ja elektroninen tilatiheys.
Isoperibolinen kalorimetri
Se on laite, jossa reaktiokenno ja pumppu upotetaan rakenteeseen, jota kutsutaan vaipaksi. Tässä tapauksessa ns. Takki koostuu vedestä, jota pidetään vakiolämpötilassa.
Kennon ja pumpun lämpötila nousee, kun lämpö vapautuu palamisprosessin aikana; mutta vesivaipan lämpötila pidetään kiinteässä lämpötilassa.
Mikroprosessori ohjaa solun ja vaipan lämpötilaa ja tekee tarvittavia korjauksia vuodonlämmöstä, joka johtuu kahden lämpötilan eroista..
Näitä korjauksia sovelletaan jatkuvasti ja lopullisella korjauksella, joka perustuu mittauksiin ennen testiä ja sen jälkeen.
Virtauskalorimetri
Caliendarin kehittämä laite sisältää laitteen kaasun siirtämiseksi säiliössä vakionopeudella. Lisäämällä lämpöä mitataan nesteen lämpötilan nousu.
Virtauskalorimetrille on ominaista:
- Vakion virtausnopeuden tarkka mittaus.
- Lämmittimen kautta nesteen sisään tuodun lämmön määrän tarkka mittaus.
- Energian tulon aiheuttama kaasun lämpötilan nousun tarkka mittaus
- Suunnittelu paineen alaisen kaasun kapasiteetin mittaamiseksi.
Kalorimetri differentiaalista skannauskalorimetriaa varten
Sille on tunnusomaista, että siinä on kaksi säiliötä: yhdessä tutkittava näyte sijoitetaan, kun taas toinen pidetään tyhjänä tai käytetään vertailumateriaalia.
Kaksi alusta lämmitetään vakioenergian nopeudella kahden riippumattoman lämmittimen avulla. Kun kahden säiliön lämmitys alkaa, tietokone kuvaa lämmittimien lämmönvirtauksen eroa lämpötilaan ja pystyy siten määrittämään lämmön virtauksen..
Lisäksi voidaan määrittää lämpötilan vaihtelu ajan funktiona; ja lopuksi kalorikapasiteetti.
sovellukset
Fysikokemiassa
-Peruskalorimetrit, tyypin kahvikuppi, mahdollistavat mitata lämpöä, jonka elin vapauttaa tai imee. Ne voivat määrittää, onko reaktio eksoterminen vai endoterminen. Lisäksi voidaan määrittää kehon spesifinen lämpö.
-Adiabaattisen kalorimetrin avulla on voitu määrittää kemiallisen prosessin entropia ja tilan elektroninen tiheys.
Biologisissa järjestelmissä
-Mikrokalorimetrejä käytetään biologisten järjestelmien tutkimiseen, jotka sisältävät molekyylien välisiä vuorovaikutuksia sekä esiintyviä molekulaarisia konformaatiomuutoksia; esimerkiksi molekyylin avautumisessa. Linja sisältää sekä differentiaalisen skannauksen että isotermisen titrauksen.
-Mikrokalorimetriä käytetään pienten molekyylien, bioterapeuttien ja rokotteiden lääkkeiden kehittämiseen.
Happipumpun kalorimetri ja kaloriteho
Monien aineiden palaminen tapahtuu happipumpun kalorimetrissä, ja sen kaloriteho voidaan määrittää. Tämän kalorimetrin avulla tutkittujen aineiden joukossa ovat: hiili ja koks; syötävät öljyt, sekä raskaat että kevyet; bensiini ja kaikki moottoripolttoaineet.
Lentokoneiden reaktoreiden polttoaineiden tyypit; polttoaineen jätteet ja jätehuolto; Elintarvikkeet ja ravintolisät ihmisravinnoksi; rehujen ja eläinten rehun lisäaineet; rakennusmateriaalit; rakettien ja ponneaineiden polttoaineet.
Samoin kalorimetria on määritetty kalorimetrialla palavien materiaalien termodynaamisissa tutkimuksissa; energian tasapainon tutkimuksessa ekologiassa; räjähdysaineissa ja lämpöjauheissa sekä perustermodynamiikan opetuksessa.
viittaukset
- Whitten, Davis, Peck & Stanley. Kemia. (8. painos). CENGAGE Learning.
- González J., Cortés L. & Sánchez A. (s.f.). Adiabaattinen kalorimetria ja sen sovellukset. Palautettu osoitteesta: cenam.mx
- Wikipedia. (2018). Calorimeter. Haettu osoitteesta: en.wikipedia.org
- Helmenstine, Anne Marie, Ph.D. (22. kesäkuuta 2018). Kalorimetri määritelmä kemiassa. Haettu osoitteesta thinkco.com
- Gillespie, Claire. (11. huhtikuuta 2018). Miten kalorimetri toimii? Sciencing. Haettu osoitteesta: sciencing.com


